
 2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )
2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢,并采用新一代的氮化镓铟高亮度LED材料.下列有关说法正确的是( )| A. | 合金的熔点通常比组分金属高,硬度比组分金属小 | |
| B. | 已知Ga处于ⅢA族,可推知氮化镓化学式为Ga3N2 | |
| C. | 用金属铝与V2O5冶炼钒,铝作还原剂 | |
| D. | 合金的化学性质一般与其各成分金属的化学性质不同 |
科目:高中化学 来源: 题型:解答题
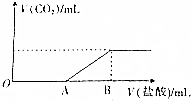 标准状况下,向100mL NaOH溶液中缓慢通入一定量的CO2气体,充分反应后,测得所得溶液M的pH>7(反应前后溶液的体积变化忽略不计),在溶液M中逐滴缓慢滴加1mol•L-1 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示,已知图中B点的位置固定,V(B)=300mL,而A点可在横坐标中自由移动.
标准状况下,向100mL NaOH溶液中缓慢通入一定量的CO2气体,充分反应后,测得所得溶液M的pH>7(反应前后溶液的体积变化忽略不计),在溶液M中逐滴缓慢滴加1mol•L-1 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示,已知图中B点的位置固定,V(B)=300mL,而A点可在横坐标中自由移动.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HCl>HBr>HI | B. | 原子半径:Na>Mg>Al | ||
| C. | 还原性:PH3>H2S>HC1 | D. | 结合H+能力:CH3COO->HCO3->ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,已知断裂1mol B-B吸收167kJ的热量,生成1mol B≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:N4(g)═2N2(g)△H=-882 kJ/mol;
,已知断裂1mol B-B吸收167kJ的热量,生成1mol B≡B放出942kJ热量.试写出由B4气态分子变成B2气态分子的热化学方程式:N4(g)═2N2(g)△H=-882 kJ/mol;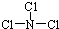 ,X与水反应的化学方程式是NCl3+3H2O═NH3+3HClO;
,X与水反应的化学方程式是NCl3+3H2O═NH3+3HClO;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2L | B. | 2.24L | C. | 3.36L | D. | 8.96L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 +H2O,H中的官能团有氯原子、羟基、醚键(填名称),与E具有相同官能团的E的同分异构体还有
+H2O,H中的官能团有氯原子、羟基、醚键(填名称),与E具有相同官能团的E的同分异构体还有


 (其中任意两个)(任写两个,不考虑立体结构);
(其中任意两个)(任写两个,不考虑立体结构); .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绿色化学的核心是利用化学原理从源头上减少和消除工农业生产对环境的污染 | |
| B. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | PM2.5是指大气中直径接近于2.5×10-6m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成混合物具有丁达尔效应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com