
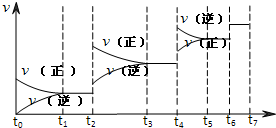
 可逆反应C(s)+H2O(g)?H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图.
可逆反应C(s)+H2O(g)?H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图.

科目:高中化学 来源: 题型:
| A、①>②>④>③ |
| B、①>②>③>④ |
| C、④>①>③>② |
| D、④>①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
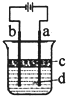 由于Fe(OH)2 极易被氧化;所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用图所示实验装置则可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.
由于Fe(OH)2 极易被氧化;所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用图所示实验装置则可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=3的醋酸与pH=11的NaOH溶液等体积混合后,溶液的pH一定小于7 |
| B、不能使酚酞试液变红的溶液一定呈酸性 |
| C、pH=5的溶液和pH=3的溶液相比,前者c(OH-)是后者的100倍 |
| D、在1mol?L-1的氨水中,改变外界条件使c(NH4+)增大,溶液的pH不一定增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| MX |
| VN |
| A、以g为单位V L该气体的质量 |
| B、以g为单位1L该气体的质量 |
| C、1 L该气体中所含的分子数 |
| D、以L为单位lmol该气体的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.3克金属钠变为钠离子失去的电子数目为0.1NA |
| B、18克水所含有的电子数目为NA |
| C、常温常压下,11.2L氯气所含的原子数目为NA |
| D、2.8克N2和CO混合气体的原子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将0.1mol CO2通入足量NaOH溶液,则溶液中阴离子数目为0.1NA |
| B、标准状况下,将11.2L的Cl2通入足量的NaOH溶液中,转移的电子数为NA |
| C、0.1mol N2与足量H2反应,转移的电子数为0.6NA |
| D、标准状况下,1.12L HCHO中C原子的数目为0.05NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、LiH与D2O反应,所得氢气的摩尔质量为4g/mol |
| B、1 mol LiAlH4在125℃完全分解,转移3 mol电子 |
| C、LiAlH4溶于适量水得无色溶液,则化学方程式可表示为:LiAlH4+2H2O=LiAlO2+4H2↑ |
| D、LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若维持温度不变,起始时②中投人3mol A、1 mol B;③中投入3 mol A、l mol B和2mol C,则达到平衡时,两容器中B的转化率②=③ |
| B、若起始温度相同,分别向三个容器中充入3 mol A和1mol B,则达到平衡时各容器中C物质的百分含量由大到小的顺序为③>②>① |
| C、若起始温度相同,分别向三个容器中充入1 mol A和1molB则达到平衡时各容器中C物质的百分含量一定相同 |
| D、若起始温度相同,分别向三个容器中充入3a mol A和a molB则达到平衡时各容器中A物质的转化率一定相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com