
��ҵ���õ�ⷨ�����������Է�ˮ���õ�����Ni��ԭ����ͼ��ʾ��
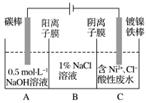
����˵������ȷ����(����)
��֪����Ni2������������Һ�з���ˮ��
�������ԣ�Ni2��(��Ũ��)��H����Ni2��(��Ũ��)
A��̼���Ϸ����ĵ缫��Ӧ��4OH����4e��===O2����2H2O
B���������У�B��NaCl��Һ�����ʵ���Ũ�Ƚ����ϼ���
C��Ϊ�����Ni�IJ��ʣ�����������Ҫ���Ʒ�ˮpH
D������ͼ��������Ĥȥ������A��B���Һϲ������ⷴӦ�ܷ���ʽ�����ı�
�𰸡�B
�������缫��ӦʽΪ
������4OH����4e��===2H2O��O2��
������Ni2����2e��===Ni
2H����2e��===H2��
A����ȷ��B�����C��Ni2����H�����ϼ��٣�Cl��ͨ��������Ĥ��C����B��A��OH�����ϼ��٣�Na��ͨ��������Ĥ��A����B������B��NaCl��Һ�����ʵ���Ũ�Ȳ���������C�����H���������Դ���Ni2��(��Ũ��)�������ԣ�����Ϊ�����Ni�IJ��ʣ���������Ҫ���Ʒ�ˮ��pH��D���ȥ��������Ĥ��������Cl���ŵ�����Cl2����Ӧ�ܷ���ʽ�����ı䣬��ȷ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������Ҫ������Դ��������Ϊ�������õĹؼ��������ǵ�ǰ��ע���ȵ�֮һ��
(1)���������ȼ�ϣ���ȼ�ղ���Ϊ________________��
(2)NaBH4��һ����Ҫ�Ĵ������壬����ˮ��Ӧ�õ�NaBO2���ҷ�Ӧǰ��B�Ļ��ϼ۲��䣬�÷�Ӧ�Ļ�ѧ����ʽΪ________________________________________________________________________
________________________________________________________________________��
��Ӧ����1 mol NaBH4ʱת�Ƶĵ�����ĿΪ________________________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡���ѧ���ļ������γ�(���)1 mol��ѧ��ʱ�ͷ�(������)����������֪����P4O6�ķ��ӽṹ����ͼ��ʾ �����ṩ���»�ѧ���ļ�������(kJ��mol��1)��P��P��198��P��O��360��O===O��497.3��
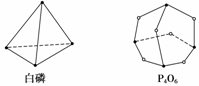
��Ӧ��P4(����)��3O2===P4O6�������仯Ϊ(����)
A���ͷ�1 640.1 kJ������
B������1 640.1 kJ������
C���ͷ�126.3 kJ������
D������126.3 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ͨ������������������������ˮ�����ٷ�Һ�ŷŶԻ�������Ⱦ��ͬʱ����K2Cr2O7��ʵ���ҶԺ�����Һ(����Cr3����Fe3����K����SO ��NO
��NO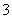 ������Cr2O
������Cr2O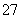 )�����������ù������£�
)�����������ù������£�

��֪����Cr(OH)3��OH��===CrO ��2H2O��
��2H2O��
��2CrO ��3H2O2��2OH��===2CrO
��3H2O2��2OH��===2CrO ��4H2O��
��4H2O��
��H2O2�����������¾��л�ԭ�ԣ��ܽ���6��Cr��ԭΪ��3��Cr��
(1)ʵ��������KOHŨ��Ϊ6 mol·L��1������KOH��������250 mL 6 mol·L��1��KOH��Һ�����ձ����������⣬�������õ��IJ���������________��
(2)��Һ���ữǰ�����м��ȵ�Ŀ����________����ԡ�����˺�Ӧ��������ˮϴ��K2Cr2O7����Ŀ����________________________��
(3)�±���������ʵ��ܽ�����ݣ�
| ���� | 0 �� | 20 �� | 40 �� | 60 �� | 80 �� | 100 �� |
| KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 | 56.3 |
| K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
| K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 | 102.0 |
| KNO3 | 13.9 | 31.6 | 61.3 | 106 | 167 | 246.0 |
�����ܽ�����ݣ�����������������Ϊ��__________________����__________��
(4)��ȡ��Ʒ�ظ��������2.000 g���250 mL��Һ��ȡ��25.00 mL����ƿ�У�����10 mL 2 mol·L��1 H2SO4�������⻯��(���Ļ�ԭ����ΪCr3��)�����ڰ���5 min��Ȼ�����100 mLˮ������3 mL����ָʾ������0.120 0 mol·L��1 Na2S2O3����Һ�ζ�(I2��2S2O ===2I����S4O
===2I����S4O )��
)��
����ʵ���й���ȥNa2S2O3����Һ30.00 mL�����ò�Ʒ���ظ���صĴ���Ϊ________(�������������������ʲ����뷴Ӧ)��
�����ζ�����ʹ��ǰδ��Na2S2O3����Һ��ϴ����õ��ظ���صĴ��Ƚ�________(�ƫ�ߡ�����ƫ�͡����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������缫����500 mL CuSO4��Һ�н��е�⣬ͨ��һ��ʱ���ijһ�缫����0.064 g(����ʱ�õ缫�������������Ҳ�����ˮ�����Һ����仯)����ʱ��Һ��������Ũ��ԼΪ(����)
A��4��10��3 mol·L��1 B��2��10��3 mol·L��1
C��1��10��3 mol·L��1 D��1��10��7 mol·L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ��ʾ�ĸ�����ʴ�У�����˵����ȷ����(����)
 ��
��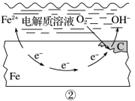
A��̼���淢��������Ӧ
B����������ʴ�����ղ���ΪFeO
C�������и�����Ʒ�ĸ�ʴ��ͼ����ʾΪ��
D��ͼ���У�������ӦʽΪO2��4e����2H2O===4OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ʊ������̵�ʵ��װ����ͼ��������ϡ����Ϊ���Һ�������������̺�������ҺΪ���Һ�����װ���м�ͷ��ʾ��Һ���������ƶ��ķ�������˵������ȷ����(����)
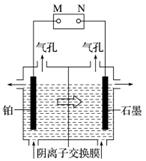
A��M�ǵ�Դ�ĸ���
B����������ݳ����������Ϊ������H2
C�������з������ܷ�ӦΪMnSO4��2H2O MnO2��H2����H2SO4
MnO2��H2����H2SO4
D�����������ӽ���Ĥ���������ӽ���Ĥ���������ܵõ�MnO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������һ�������Դ����������ȡ�봢��������Դ����������о��ȵ㡣
��֪��CH4(g)��H2O(g)===CO(g)��3H2(g)
��H��206.2 kJ·mol��1
CH4(g)��CO2(g)===2CO(g)��2H2(g)
��H��247.4 kJ·mol��1
2H2S(g)===2H2(g)��S2(g)
��H��169.8 kJ·mol��1
(1)�Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����
CH4(g)��H2O(g)��Ӧ����CO2(g)��H2(g)���Ȼ�ѧ����ʽΪ________________________________________________________________________��
(2)H2S�ȷֽ�����ʱ������Ӧ����ͨ��һ������������ʹ����H2Sȼ�գ���Ŀ����____________________________��ȼ�����ɵ�SO2��H2S��һ����Ӧ���������ڳ����¾������壬д���÷�Ӧ�Ļ�ѧ����ʽ��_____________________________________________��
(3)H2O���ȷֽ�Ҳ�ɵõ�H2��������ˮ�ֽ���ϵ����Ҫ���������������¶ȵĹ�ϵ����ͼ��ʾ��ͼ��A��B��ʾ������������________________________��
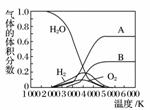
(5)Mg2Cu��һ�ִ���Ͻ�350 ��ʱ��Mg2Cu��H2��Ӧ������MgCu2�ͽ���һ�ֽ���Ԫ�ص��⻯��(���������������Ϊ0.077)��Mg2Cu��H2��Ӧ�Ļ�ѧ����ʽΪ________________________________________________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com