
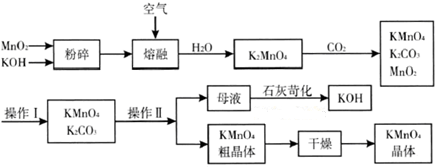
���� ��MnO2��KOH���飬Ŀ��������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ�Ȼ��������ڲ�ͨ���������������ͼ֪�����߷�Ӧ����K2MnO4������Ԫ���غ�֪������H2O��K2MnO4��CO2��Ӧ����KMnO4��K2CO3��MnO2��KMnO4��K2CO3������ˮ��MnO2������ˮ����KMnO4��K2CO3��MnO2����ˮȻ����˵õ�KMnO4��K2CO3�����Һ���ٸ���KMnO4��K2CO3�ܽ�Ȳ�����ü���Ũ������ȴ�ᾧ�ķ������KMnO4���壬ĸҺ�к���K2CO3������CaO��������ӦK2CO3+CaO+H2O=CaCO3��+2KOH���Ӷ��õ�KOH��
��KMnO4����ϴ�Ӹ���õ�������KMnO4���壻
��1��KMnO4����ǿ�����Զ�ɱ��������
��2����������ͼ֪��KOH��MnO2������ѭ�����ã�
��3������ԭ���غ�֪��1molMnO2���Ƶ�1molK2MnO4��K2MnO4��CO2��Ӧ����KMnO4��K2CO3��MnO2����Ӧ����ʽΪ3K2MnO4+2CO2=2KMnO4+MnO2+2K2CO3��
��4��ʯ��ʯ��̼�����ƶ��ܺ�ϡ������ȡ������̼������ȡ�Ķ�����̼�к���HCl��ϡ�����ʯ��ʯ��Ӧ������������ƶ���ֹ��Ӧ��ϡ�����̼�����Ʒ�Ӧ���ɶ�����̼����ϡ����û�лӷ��ԣ�
��5���������������Һ���ù��˷���������������ˮ���������ʸ������ܽ�Ȳ����Բ��������ᾧ������
��� �⣺��MnO2��KOH���飬Ŀ��������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ�Ȼ��������ڲ�ͨ���������������ͼ֪�����߷�Ӧ����K2MnO4������Ԫ���غ�֪������H2O��K2MnO4��CO2��Ӧ����KMnO4��K2CO3��MnO2��KMnO4��K2CO3������ˮ��MnO2������ˮ����KMnO4��K2CO3��MnO2����ˮȻ����˵õ�KMnO4��K2CO3�����Һ���ٸ���KMnO4��K2CO3�ܽ�Ȳ�����ü���Ũ������ȴ�ᾧ�ķ������KMnO4���壬ĸҺ�к���K2CO3������CaO��������ӦK2CO3+CaO+H2O=CaCO3��+2KOH���Ӷ��õ�KOH��
��KMnO4����ϴ�Ӹ���õ�������KMnO4���壻
��1��KMnO4����ǿ�����Զ�ɱ��������
a��84����Һ��NaClO��Һ������ǿ�����Զ�ɱ������������ȷ��
b��������ͨ������ϸ�����ڣ�ʹϸ�����������̣����ԣ����Ӷ�ɱ��ϸ�����ʴ���
c�����������ж����ܹ�����ù����ϸ����������ɱ���������ʴ���
d���ƾ���ͨ������ϸ�����ڣ�ʹϸ�����������̣����ԣ����Ӷ�ɱ��ϸ�����ʴ���
��ѡa��
��2����������ͼ֪����ʼ��Ӧ����KOH��MnO2��̼��غ�ʯ�ҿ����õ�KOH������غͶ�����̼��Ӧ����MnO2������KOH��MnO2������ѭ�����ã�
�ʴ�Ϊ��KOH��MnO2��
��3������ԭ���غ�֪��1molMnO2���Ƶ�1molK2MnO4��K2MnO4��CO2��Ӧ����KMnO4��K2CO3��MnO2����Ӧ����ʽΪ3K2MnO4+2CO2=2KMnO4+MnO2+2K2CO3��3mol���������2mol������أ�����1mol������������$\frac{2}{3}$mol������أ�
�ʴ�Ϊ��$\frac{2}{3}$��
��4��ʯ��ʯ��̼�����ƶ��ܺ�ϡ������ȡ������̼��������лӷ��ԣ�������ȡ�Ķ�����̼�к���HCl�����¶�����̼��������ϡ�����ʯ��ʯ��Ӧ������������ƶ���ֹ��Ӧ��ϡ�����̼�����Ʒ�Ӧ���ɶ�����̼����ϡ����û�лӷ��ԣ�������ȡ�Ķ�����̼�ϴ�������ѡcd��
��5���������������Һ���ù��˷�����KMnO4��K2CO3������ˮ��MnO2������ˮ�����Բ���IΪ���ˣ�����������ˮ���������ʸ������ܽ�Ȳ����Բ��������ᾧ������KMnO4��K2CO3��������ˮ�������ܽ�Ȳ�ͬ�����Բ��������KMnO4��K2CO3���������ܽ���ϵIJ��죬����Ũ���ᾧ�����ȹ��˵õ�KMnO4�־��壬
�ʴ�Ϊ�����ˣ��ܽ�ȣ�Ũ���ᾧ��
���� ���⿼�������Ʊ�ʵ�鷽����ƣ�Ϊ�߿���Ƶ�㣬���ؿ����������ʡ����������������֪ʶ�㣬��ȷ����ͼ�и������ڷ����ķ�Ӧ�����������ǽⱾ��ؼ���ע�⣨3����������е�MnԪ�ز�����ȫת����������ػ�����ת�������������У�Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
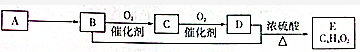
| A�� | B�к��еĹ�����Ϊ�ǻ� | B�� | ����̼������Һ����B��D | ||
| C�� | D�к���C�TO����E������Ϊ�������� | D�� | B+D��E��Ӧ��װ����ͼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
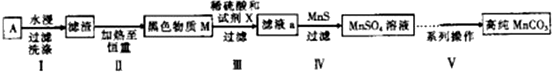
 �������ƣ�NaClO2����һ����Ҫ�ĺ�������������Ҫ����ˮ�������Լ�ɰ�ǡ���֬��Ư����ɱ������ͼ�ǹ������ⷨ�����������ƵĹ�������ͼ��
�������ƣ�NaClO2����һ����Ҫ�ĺ�������������Ҫ����ˮ�������Լ�ɰ�ǡ���֬��Ư����ɱ������ͼ�ǹ������ⷨ�����������ƵĹ�������ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ���� | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | �Լ�X | MnSO4/g |
| 1 | � | 2.3595 |
| 2 | ���� | 2.7184 |
| 3 | ������ | 2.9911 |
| 4 | 30%�������� | 3.7349 |
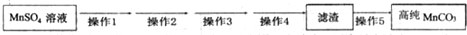
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� Al��OH��3+3H+�������ӷ���ʽ��ʾ����
Al��OH��3+3H+�������ӷ���ʽ��ʾ����| X | ||||
| Y | Z | W |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com