
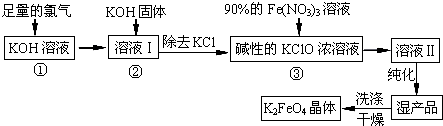
���� ��������ͨ������������Һ�е��·�Ӧ���ɴ�����ء��Ȼ��غ�ˮ����������������س�ȥ�Ȼ��صõ����Դ������Ũ��Һ������������Ũ��Һ�õ���Һ����ϴ�Ӹ���õ�������أ�
��1��������Ŀ��Ϣ��������ԭ��Ӧ�л��ϼ۷����仯ȷ�������Լ����ӵ�ʧ�غ�������غ�����ƽ�����ݻ��ϼ����ߣ���ԭ�����õ��������
��2������������������ͼ���ڢٲ������������ڢ۲���Ҫ�������������¶Ƚϸ�ʱKOH ��Cl2 ��Ӧ���ɵ���KClO3��������ԭ��Ӧ�л��ϼ������н���
��3��������Ŀ��Ϣ��������ԭ��Ӧ�л��ϼ۷����仯ȷ�������Լ����ӵ�ʧ�غ�������غ�����ƽ��
��4���������һ�ε�ϴ������Cl-���ɣ�
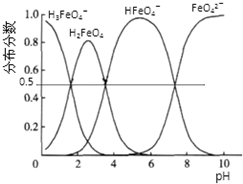
��5��A����ͬPHֵʱ����Һ����Ԫ�صĴ�����̬����������ͬ��������PHֵ����6ʱ����ֻ��������̬��
B������ͼƬ֪�����ݲ�ͬpHʱ��HFeO4-�ı仯ͼ���жϣ�
C����pH=8��������Һ�м�KOH��Һ��������Ӧ�����ӷ���ʽΪ��HFeO4-+OH-=FeO42-+H2O��
��� �⣺��1������Ŀ��Ϣ��������ԭ��Ӧ�л��ϼ۷����仯ȷ�������У�KClO3��KCl��H2O�����ݵ��ӵ�ʧ�غ�������غ�����ƽ���ɵ�6KOH+3Cl2$\frac{\underline{\;\;��\;\;}}{\;}$KClO3+5KCl+3H2O��Cl2�������������ǻ�ԭ�����Ȼ��ϼ����ߣ��õ� KClO3��KClO3�ǻ�ԭ���
�ʴ�Ϊ��6KOH+3Cl2$\frac{\underline{\;\;��\;\;}}{\;}$KClO3+5KCl+3H2O��KClO3��
��2��A������������������ͼ���ڢٲ���������������KOH�����������Ӧ����KClO����A��ȷ��
B�����¶Ƚϸ�ʱKOH ��Cl2 ��Ӧ���ɵ���KClO3��������KClO����B����
C���ڢ۲���Ҫ�������������Լ�Ҫ��������C��ȷ��
D��KClO3ת��Ϊ KClO�����ϼ�ֻ����������D����
�ʴ�Ϊ��A��C��
��3������Ŀ��Ϣ��������ԭ��Ӧ�л��ϼ۷����仯ȷ���ҳ���Ӧ�Fe3+��ClO-�������FeO42-��Cl-�����ݵ��ӵ�ʧ�غ�������غ�����ƽ���ɵ�2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O��
�ʴ�Ϊ��2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O��
��4����ֻҪ�������һ�ε�ϴ������Cl-������֤��K2FeO4�����Ѿ�ϴ�Ӹɾ�������Ϊ�Թ�ȡ�������һ�ε�ϴ��Һ��������������Һ���ް�ɫ�������ѱ�ϴ����
�ʴ�Ϊ�����Թ�ȡ�������һ�ε�ϴ��Һ��������������Һ���ް�ɫ�������ѱ�ϴ����
��5��A����ͬPHֵʱ����Һ����Ԫ�صĴ�����̬����������ͬ��������PHֵ����6ʱ����ֻ��������̬����A����
B��ͼ�������֪��pH��2�仯Ϊ10ʱ��HFeO4-�ķֲ�������������С����B��ȷ��
C����pH=8��������Һ�м�KOH��Һ��������Ӧ�����ӷ���ʽΪ��HFeO4-+OH-=FeO42-+H2O����C����
�ʴ�Ϊ��B��
���� ���⿼��ѧ���Ķ���Ŀ��ȡ��Ϣ���������Թ������̵������������Ŀ��ơ������ʵ���Ũ������ȣ��Ѷ��еȣ���Ҫѧ��������ʵ�Ļ���֪ʶ���������֪ʶ��������������ע�����֪ʶ�����գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮ�������c��OH-��=1��10-13mol/L����Һ�У�Na+��Al3+��Cl-��NO3- | |
| B�� | �ڼ��������ܲ���H2����Һ�У�NH4+��Fe2+��SO42-��NO3- | |
| C�� | �ڳ���������Һ�У�Cu2+��K+��SO42-��Cl- | |
| D�� | ����ʹ���ȱ��ɫ����Һ�У�Na+��CO32-��NO3-��K+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
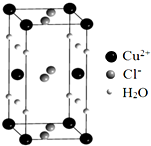 �������İ�ˮ�ӵ�����ͭ��Һ�У���Һ���ձ������ɫ�����������Ҵ�����������Cu��NH3��4SO4•H2O•SO42-
�������İ�ˮ�ӵ�����ͭ��Һ�У���Һ���ձ������ɫ�����������Ҵ�����������Cu��NH3��4SO4•H2O•SO42-�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 30% | B�� | 40% | C�� | 50% | D�� | 60% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijѧ����0.100 0mol•L-1�������Һ�ⶨij�ռ���Ʒ�Ĵ��ȣ����ʲ������ᷴӦ����ʵ�鲽�����£�
ijѧ����0.100 0mol•L-1�������Һ�ⶨij�ռ���Ʒ�Ĵ��ȣ����ʲ������ᷴӦ����ʵ�鲽�����£�| �ζ����� | ����Һ��� | �����������mL�� | |
| �ζ�ǰ������mL�� | �ζ��������mL�� | ||
| ��һ�� | 20.00 | 0.20 | 20.38 |
| �ڶ��� | 20.00 | 4.00 | 24.20 |
| ������ | 20.00 | 2.38 | a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
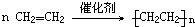
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
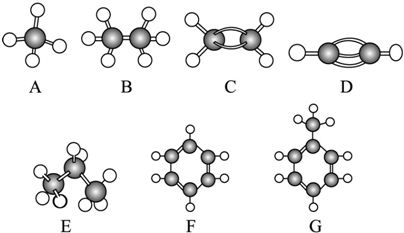
 ±��Ԫ�صĵ��ʺͻ�����ܶ࣬���ǿ���������ѧ���ʽṹ�����ʵ����֪ʶȥ��ʶ�����⣮
±��Ԫ�صĵ��ʺͻ�����ܶ࣬���ǿ���������ѧ���ʽṹ�����ʵ����֪ʶȥ��ʶ�����⣮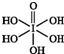 ����HIO4��ǰ��Ϊ��Ԫ�ᣬ����ΪһԪ�ᣮ��Ƚ϶�������ǿ����H5IO6��HIO4���������������=������
����HIO4��ǰ��Ϊ��Ԫ�ᣬ����ΪһԪ�ᣮ��Ƚ϶�������ǿ����H5IO6��HIO4���������������=�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ԫ�������� | B�� | �����ԭ��ѧ˵ | ||
| C�� | ������ϡ������ | D�� | ����˷���ѧ˵ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com