
【题目】为了保护环境,充分利用资源,某研究小组通过如下简化流程,将工业制硫酸的硫铁矿渣(铁主要以Fe2O3存在)转变成重要的化工原料FeSO4(反应条件略)。
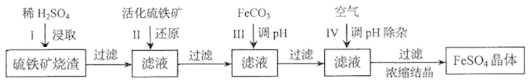
活化硫铁矿还原Fe3+的主要反应为:FeS2+7Fe2(SO4)3+8H2O=15FeSO4+8H2SO4,不考虑其他反应。请回答下列问题:
(1)第Ⅰ步H2SO4与Fe2O3反应的离子方程式是_____________________。
(2)检验第Ⅱ步中Fe3+是否完全还原,应选择_________________(填字母编号)。
A.KMnO4溶液 B.淀粉-KI溶液 C.KSCN溶液
(3)第Ⅲ步加FeCO3调溶液pH到5.8左右,然后在第Ⅳ步通入空气使溶液pH降到5.2,此时Fe2+不沉淀,滤液中铝、硅杂质除尽。通入空气引起溶液pH降低的原因是_______________。
(4)FeSO4在一定条件下可制得FeS2(二硫化亚铁)纳米材料。该材料可用于制造高容量锂电池,电池放电时的总反应为4Li+ FeS2=Fe+2Li2S,正极反应式是___________。
(5)FeSO4可转化为FeCO3,FeCO3在空气中加热反应可制得铁系氧化物材料。
已知25℃,101kPa时:4Fe(s)+ 3O2 (g)=2Fe2O3(s)H=-1648kJ/mol
C(s)+O2(g)=CO2(g)H =-392kJ/mol
2Fe(s)+2C(s)+3O2(g)=2FeCO3(s)H =-1480kJ/mol
FeCO3在空气中加热反应生成Fe2O3的热化学方程式是______________。
(6)假如烧渣中的铁全部视为Fe2O3,其含量为p。将b kg质量分数为c的硫酸加入到a kg烧渣中浸取,铁的浸取率为q,其他杂质浸出消耗的硫酸以及调pH后溶液呈微酸性所残留的硫酸忽略不计。按上述流程,第Ⅲ步应加入FeCO3___________kg。
【答案】Fe2O3+6H+=2Fe3++3H2O BC Fe2+被氧化为Fe3+,Fe3+水解产生H+ FeS2+4e-=Fe+2S2- 4FeCO3(s)+O2(g) =2Fe2O3(s)+ 4CO2(g) H=-256kJ/mol ![]() -
-![]()
【解析】
硫铁矿烧渣用硫酸浸取,过滤后滤液中含有硫酸铁和未反应的硫酸,用活化硫铁矿还原铁离子后过滤,向滤液中加入碳酸亚铁调节溶液pH,过滤后再通入空气,调节溶液的pH,除去溶液中杂质离子,过滤浓缩结晶得到硫酸亚铁晶体。
硫铁矿烧渣用硫酸浸取,过滤后滤液中含有硫酸铁和未反应的硫酸,用活化硫铁矿还原铁离子后过滤,向滤液中加入碳酸亚铁调节溶液pH,过滤后再通入空气,调节溶液的pH,除去溶液中杂质离子,过滤浓缩结晶得到硫酸亚铁晶体。
(1)硫酸和氧化铁反应生成硫酸铁和水,离子方程式为:Fe2O3+6H+=2Fe3++3H2O。
(2)检验Fe3+是否完全还原即检验还原后的溶液中是否含Fe3+,淀粉碘化钾可以和铁离子反应生成碘单质,碘单质遇淀粉显蓝色;硫氰化钾可以检验铁离子,溶液显红色;KMnO4溶液与Fe3+不反应,不能检验Fe3+;答案选BC。
(3)氧气可以将Fe2+被氧化为Fe3+, Fe3+水解产生H+,使溶液的pH降低。
(4)电池放电时的总反应为4Li+ FeS2=Fe +2Li2S,正极发生得电子的还原反应,所以是二硫化亚铁得到电子生成铁和硫离子,电极反应式为:FeS2+4e-=Fe+2S2-。
(5)将已知热化学方程式编号
①4Fe(s)+ 3O2(g)=2Fe2O3(s)H=-1648kJ/mol
②C(s)+O2(g)=CO2(g)H =-392kJ/mol
③2Fe(s)+2C(s)+3O2(g)=2FeCO3(s)H =-1480kJ/mol
根据盖斯定律,①-③×2+②×4即得,4FeCO3(s)+O2(g)=2Fe2O3(s)+ 4CO2(g)H=-1648kJ/mol-2×(-1480kJ/mol)+4×(-392kJ/mol)=-256kJ/mol。
(6)氧化铁含量为p,akg烧渣中氧化铁的质量为ap×103g,铁的浸取率为q,则参与反应的氧化铁的质量为ap×103×qg,物质的量为![]() mol;硫酸的物质的量为
mol;硫酸的物质的量为![]() mol;加入碳酸亚铁,浸取时加入的硫酸,活化硫铁矿还原铁离子时生成的硫酸完全转化为硫酸亚铁,根据FeS2~7Fe2(SO4)3~7Fe2O3,可知参加反应的二硫化亚铁的物质的量为硫酸铁物质的量的
mol;加入碳酸亚铁,浸取时加入的硫酸,活化硫铁矿还原铁离子时生成的硫酸完全转化为硫酸亚铁,根据FeS2~7Fe2(SO4)3~7Fe2O3,可知参加反应的二硫化亚铁的物质的量为硫酸铁物质的量的![]() ,即为
,即为![]() mol;根据硫元素守恒,硫酸亚铁的总物质的量=(
mol;根据硫元素守恒,硫酸亚铁的总物质的量=( ![]() +
+ ![]() )mol;根据铁元素守恒知碳酸亚铁的物质的量= (
)mol;根据铁元素守恒知碳酸亚铁的物质的量= ( ![]() +
+ ![]() )mol -
)mol - ![]() mol -
mol - ![]() mol,质量为 [(
mol,质量为 [( ![]() +
+ ![]() )mol -
)mol - ![]() mol -
mol - ![]() mol] ×116g/mol=(
mol] ×116g/mol=(![]() )kg。
)kg。


科目:高中化学 来源: 题型:
【题目】二氧化钛是制取航天航空工业钛合金的重要原料.用钛铁矿![]() 主要成分是钛酸亚铁
主要成分是钛酸亚铁![]() ,含少量
,含少量![]() 、MgO、
、MgO、![]() 等杂质
等杂质![]() 作原料生产金属钛和绿矾
作原料生产金属钛和绿矾![]() 等产品的一种工艺流程如下:已知:Ti有两种价态,在水溶液中主要以
等产品的一种工艺流程如下:已知:Ti有两种价态,在水溶液中主要以![]() 无色
无色![]() 、
、![]() 紫色
紫色![]() 形式存在.
形式存在.
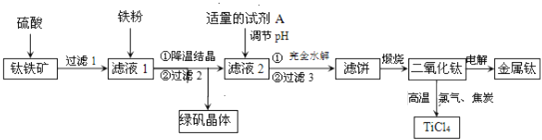
请回答下列问题:
![]() 硫酸与
硫酸与![]() 反应生成
反应生成![]() 的化学方程式是______.
的化学方程式是______.
![]() 滤液1中加入适量铁粉,至刚好出现紫色为止,此时溶液仍呈强酸性.
滤液1中加入适量铁粉,至刚好出现紫色为止,此时溶液仍呈强酸性.
已知:氧化性:![]() 则加入铁粉的作用是______.
则加入铁粉的作用是______.
![]() 滤液2中加入适量的试剂A,可选用______
滤液2中加入适量的试剂A,可选用______![]() 填编号
填编号![]() .
.
![]() 稀
稀![]() 通入
通入![]() 鼓入空气
鼓入空气
![]() 已知
已知![]() ,101kPa时,由二氧化钛制取四氯化钛所涉及的反应有:
,101kPa时,由二氧化钛制取四氯化钛所涉及的反应有:
![]() ,
,
![]() ,
,
![]()
反应![]() ______.
______.
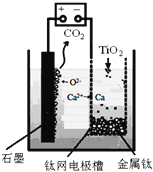
![]() 用石墨作阳极、钛网作阴极、熔融
用石墨作阳极、钛网作阴极、熔融![]() 作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.写出阴极区反应的电极总反应式是______.
作电解质,利用如图所示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.写出阴极区反应的电极总反应式是______.
![]() 假如
假如![]() 中的铁元素占矿物中铁元素总量的
中的铁元素占矿物中铁元素总量的![]() ;某次生产中,向滤液1中加入纯铁粉为bkg,得到绿矾晶体的质量为cKg,整个过程中铁元素的总利用率为
;某次生产中,向滤液1中加入纯铁粉为bkg,得到绿矾晶体的质量为cKg,整个过程中铁元素的总利用率为![]() ,Ti元素的转化率为
,Ti元素的转化率为![]() ,其他损失忽略不计.按上述流程,得到
,其他损失忽略不计.按上述流程,得到![]() ______
______![]() 用数字和字母表示
用数字和字母表示![]() 已知:
已知:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,lmol化学键分解成气态原子所需要的能量用E表示。结合表中信息判断,下列说法不正确的是

A.432kJ·mol-1>E(H—Br)>298KJ·mol-1
B.表中最稳定的共价键是H—F键
C.H2(g)→2H(g)△H=+436kJ·mol-1
D.H2(g)+F2(g)=2HF(g)△H=-25kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2被称为“空中死神”,其对环境的危害常表现为_______________。为了减少危害,人们进行了许多有益的探索和研究,并且在实际应用上取得了一定的成果。
(1)工业上常用生石灰来处理煤炭中的SO2,这是利用了SO2属于_______氧化物的性质。
(2)近年来,有人提出了一种利用电解饱和氯化钠溶液,循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:

①此种方法中,可以循环利用的物质是_____________________________。
②写出反应Ⅰ的离子方程式:_____________________________________。
(3)SO2通过下列工艺流程可制备化工原料H2SO4和清洁能源H2

下列说法中正确的是____________ 。
A. 设备A中的溴水褪色,体现了SO2的漂白性
B. 该生产工艺的优点:Br2可以循环利用,并获得清洁能源H2
C. 该工艺流程的总反应方程式为:SO2+2H2O=H2SO4+H2
D. 设备B中物质分离操作为过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车安全气囊弹出时的反应为:![]() 下列说法正确的是( )
下列说法正确的是( )
A.自然界中氮、钠、硅元素均可以游离态形式存在
B.将反应后的固体溶于适量水,静置,通入![]() ,无现象
,无现象
C.微粒的半径:![]()
D.若反应中转移![]() 电子,则消耗
电子,则消耗![]() 的质量为
的质量为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向某一元酸HR溶液中滴加一元碱BOH溶液,混合溶液的 或
或 与pH变化的关系如图所示。下列叙述正确的是
与pH变化的关系如图所示。下列叙述正确的是![]()

A.M线表示 随pH的变化
随pH的变化
B.BR溶液呈碱性
C.若温度升高,两条线均向上平移
D.常温下,![]() 溶液的
溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚是重要的有机中间体,利用二氧化碳加氢合成二甲醚能变废为宝,且可替代汽油作为新型清洁燃料。常温常压下,二氧化碳加氢可选择性生成二甲醚或一氧化碳:
①CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H1=﹣55.7kJ/mol
②2CH3OH(l)═CH3OCH3(g)+H2O(l)△H2=﹣23.4kJ/mol
③CO2(g)+H2(g)═CO(g)+H2O(l) △H3
④H2O(l)=H2O(g) △H4=+44.0kJ/mol
(1)已知反应CO2(g)+H2(g)=CO(g)+H2O(g)△H,中相关的化学键键能数据如下:

由此计算△H=______,则△H3=_______。
(2)CO2(g)加氢转化为CH3OCH3(g)和H2O(l)的热化学方程式是___。
(3)合成二甲醚往往选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。硅铝比与产物选择性如图所示,图中A点和B点的平衡常数比较:KA___KB(填“>、=、<”)。根据以上两条曲线,写出其中一条变化规律:a.___。b.___。
(4)常温常压下,向一个2.00L的密闭恒容容器中加入等量2.00mol二氧化碳和氢气,平衡时二甲醚的浓度为0.150mol/L,计算此时二氧化碳的转化率及该反应的平衡常数,要求写出计算过程(计算结果保留3位有效数字)________、_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为前四周期原子序数依次增大的五种元素。A原子半径是周期表中原子半径最小的;B可以和A形成两种常见的液态化合物甲和乙,且原子个数之比分别是1:1和1:2;C、 D为同周期元素,C是所属周期的主族元素中电负性最小的;D的单质晶体是分子晶体,原子最外层有两个未成对电子;E位于周期表的ds区,E元素原子最外层有一个未成对电子。回答下列问题:
(1)E2+的简化电子排布式是__________;甲和乙沸点较高的是___________(填化学式);
(2)D与B形成常见的具有还原性的阴离子立体构型是三角锥形;则D显最高正价时与B形成的常见化合物的中心原子的杂化类型是_________
(3)同时由A、B、C、D四种元素组成的两种盐M和W,写出这两种盐溶液反应的离子方程式___________
(4)由B、D、E三种元素组成常见盐溶液丙,向丙溶液加入过量NaOH溶液可生成[E(OH)4]2-,不考虑空间构型,[E(OH)4]2-的结构可用示意图表示为__________
(5)根据周期表对角线规则,铍和铝的性质有相似性,则书写铍单质和C的最高正价氧化物对应水化物溶液发生反应的离子方程式是___________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com