
| A. | 增大C或D的浓度 | B. | 减小B或A的浓度 | C. | 减小C或D的浓度 | D. | 充入稀有气体 |
 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
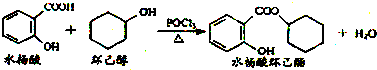
| A. | 水杨酸能分别与NaHCO3、Na2CO3溶液反应,且1 mol水杨酸分别消耗NaHCO32mol、Na2CO31mol | |
| B. | 水杨酸、环己醇和水杨酸环己酯均能与FeCl3溶液发生显色反应 | |
| C. | 1 mol水杨酸环己酯在NaOH溶液中水解时,最多消耗3 mol NaOH | |
| D. | 1 mol水杨酸跟足量浓溴水反应时,最多消耗Br2 2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘化氢的生成速率大于其分解速率 | |
| B. | 碘化氢的生成速率等于其分解速率 | |
| C. | 加催化剂不会影响达到平衡的时间 | |
| D. | 升高温度可以缩短到达平衡状态的时间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A<B<C<D | |
| B. | 非金属性:C>A | |
| C. | 最高价氧化物对应水化物的酸性:D>C | |
| D. | 单质B常温下能溶于浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可能等于7 | B. | 一定<7 | C. | 一定>7 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中的氧化剂只有Cu2O | |
| B. | 氧化产物和还原产物的物质的量之比为6:1 | |
| C. | Cu既是氧化产物又是还原产物 | |
| D. | Cu2S在反应中既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
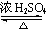 CH3COOCH2CH=CH2+H218O,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式
CH3COOCH2CH=CH2+H218O,酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式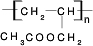 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
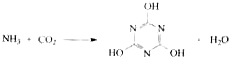 下列有关三聚氰胺的说法正确的是( )
下列有关三聚氰胺的说法正确的是( )| A. | 分子式为C3H6N3O3 | B. | 分子中既含极性键,又含非极性键 | ||
| C. | 属于共价化合物 | D. | 生成该物质的上述反应为中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com