
某一反应体系有反应物和生成物共五种物质:O2 、H2CrO4 、Cr(OH)3 、H2O 、H2 O2 已知该反应中H2O2只发生如下过程:H2O2→O2
O2 已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是___________________。
(2)该反应中,发生还原反应的过程是____________ → ________________。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目(单线桥表示)___________________。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为________ L。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届湖北省高三1月质检化学试卷(解析版) 题型:填空题
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:
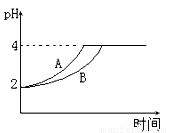
(1)常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。则图中表示醋酸溶液中pH变化的曲线是 填“A”或“B”)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为 m2。 则 m1 m2 ( 选填“<”、“=”、“>”)。[来
(2)在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g)  CH3OH(g)。升高温度,K值 (填“增大”、“减小”或“不变”)。在500℃,从反应开始到达到平衡,用氢气浓度变化表示的平均反应速率v(H2)= 。
CH3OH(g)。升高温度,K值 (填“增大”、“减小”或“不变”)。在500℃,从反应开始到达到平衡,用氢气浓度变化表示的平均反应速率v(H2)= 。
(3)某温度下Ksp[ Mg(OH)2] = 2×10 -11,若该温度下某MgSO4溶液里c(Mg 2+) =0.002 mol·L-1,如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于 ;该温度 下,在0.20L的0.002mol/LMgSO4溶液中加入等体积的0.10mol/L的氨水溶液,该温度下电离常数Kb(NH3·H2O)=2×10-5,试计算 (填“有”或“无”) Mg(OH)2沉淀生成?
下,在0.20L的0.002mol/LMgSO4溶液中加入等体积的0.10mol/L的氨水溶液,该温度下电离常数Kb(NH3·H2O)=2×10-5,试计算 (填“有”或“无”) Mg(OH)2沉淀生成?
(4)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。在分 析该溶液遇酚酞呈红色原因时,
析该溶液遇酚酞呈红色原因时, 甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致。
甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致。 请你设计一个
请你设计一个 简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论) 。
简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论) 。
查看答案和解析>>
科目:高中化学 来源:2017届北京市昌平区高三上学期期末化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数,下列说法正确的是
A.3.2gO2和O3的混合物中含有的氧原子数目为0.2NA
B.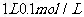 的醋酸溶液中含有氢离子数目为0.1NA
的醋酸溶液中含有氢离子数目为0.1NA
C.标准状况下,2.24LCCl4含碳原子数目为0.1NA
D.将5.85 g NaCl固体溶解在100 mL水中,得到溶液中c(Na+)=1mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省长春市五县高二上期末化学试卷(解析版) 题型:选择题
工业废气H2S经资源化利用后可回收能量并得到单质硫。反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) △H=-632kJ·mol-1。H2S燃料电池的工作原理如图所示。下列说法不正确的是( )
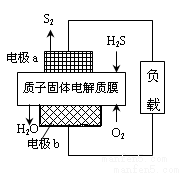
A.电极a为电池的负极
B.电极b上发生的电极反应为O2+4H++4e-=2H2O
C.若电路中通过2mol电子,则电池内部释放632kJ热能
D.若有17gH2S参与反应,则会有1molH+经质子膜进入正极区
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省长春市五县高二上期末化学试卷(解析版) 题型:选择题
常温下,物质的量浓度均为0.1mol·L-1的下列四种溶液,其中pH最小的是( )
A.NaCl B.Ba(OH)2 C.NH4Al(SO4)2 D.Na3PO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
已知在相同条件下进行下列反应:①Cl2+2KBr=2KCl+Br2;②KClO3 +6HCl=3Cl2+KCl +3H2O;③2KBrO3 +Cl2=Br2 + 2KClO3。下列说法正确的是:
A.上述三个反应都有单质生成,所以都是置换反应
B.反应①和反应③中均生成Br2,溴元素发生的变化相同
C.反应②中被氧化与被还原物质的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为10mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
在酸性溶液中能大量共存,并且溶液为无色透明的是( )
A.K+、Ca2+、HCO3-、Cl- B.Cu2+、Na+、NO3-、Cl-
C.Na+、K+ 、Mg2+、SO42- D.Mg2+、Fe3+、Cl-、OH-
、Mg2+、SO42- D.Mg2+、Fe3+、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:填空题
科学家利用太阳能分解 水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以
水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以 甲醇为燃料的燃料电池。请回答下列问题:
甲醇为燃料的燃料电池。请回答下列问题:
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知,CH3OH(g)的燃烧热__________(填“大于”、“等于”或小于”)192.9kJ/mol。已知水的汽化热为44 kJ/mol,则表示氢气燃烧热的热化学方程式为__________________________。
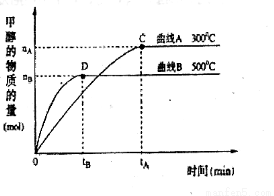
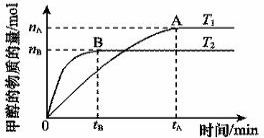
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃)该反应为_________反应(填“放热”或“吸热”);在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平 衡后,若CO2转化率为a,则容器内的压强与起始压强之比为____________________。
衡后,若CO2转化率为a,则容器内的压强与起始压强之比为____________________。
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上第二次段考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是 ( )
A.Cl2与水反应:Cl2+ H2O = Cl-+ClO-+ 2H+
B.Fe溶于稀硝酸:2Fe+6H+ = 2Fe3++3H2↑
C.烧碱溶液中加入铝片:2Al+2OH-+2H2O = 2AlO2-+3H2↑
D.在稀氨水中通入过量CO2:2NH3·H2O+CO2 = 2NH4++CO32-+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com