
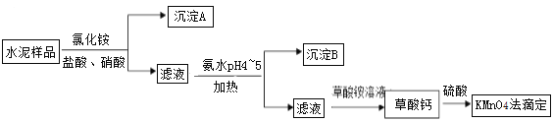
【题目】港珠澳大桥水泥的使用量约198万吨。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
下列叙述正确的是
A. 水泥、玻璃、陶瓷为传统的硅酸盐材料,三者的原料都主要为SiO2
B. 沉淀A主要成分为SiO2,沉淀B为Fe(OH)3、Al(OH)3
C. 为了加快溶解速率,使用盐酸代替硫酸处理草酸钙
D. 草酸钙易溶于水
【答案】B
【解析】
A.水泥、玻璃、陶瓷均为硅酸盐工业产品,所以主要成分是硅酸盐,三者的原料不同,三者的原料并非都主要为SiO2,例如:陶瓷的主要原料有黏土等,水泥的主要原料有石灰石和黏土(铝硅酸盐),故A错误;
B.水泥样品的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物,加入氯化铵、盐酸和硝酸,由于二氧化硅与酸不反应,则得到的沉淀A为SiO2,滤液中含有Ca2+、Fe3+、Al3+、Mg2+等离子,加入氨水调节pH到4~5之间,可生成Al(OH)3、Fe(OH)3沉淀,则沉淀B为Fe(OH)3、Al(OH)3,故B正确;
C.使用盐酸代替硫酸处理草酸钙,在溶液中剩余的盐酸也能被高锰酸钾氧化,从而干扰草酸的测定,进而使测得的钙的含量产生误差,故C错误;
D.草酸钙是难溶于水的白色固体,故D错误;
本题答案为B。


科目:高中化学 来源: 题型:
【题目】利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。当电池工作时,有关说法正确的是( )

A.铝罐将逐渐被腐蚀
B.碳粒和碳棒上发生的反应为O2+2H2O-4e-=4OH-
C.碳棒应与玩具电机的负极相连
D.该电池工作一段时间后碳棒和碳粒的质量会减轻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式及有关应用的叙述中,正确的是
A. 甲烷的燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2(g) ═ CO2(g) + 2H2O(g) △H = -890.3kJmol-1
B. 已知强酸与强碱在稀溶液里反应的中和热为57.3kJmol-1,则1/2H2SO4(aq)+1/2Ba(OH)2(aq)═1/2BaSO4(s)+H2O(l) △H = -57.3kJmol-1
C. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) △H = -38.6kJmol-1
2NH3(g) △H = -38.6kJmol-1
D. 已知25℃、101KPa条件下:4Al(s) + 3O2(g) ═ 2A12O3(s) △H = -2834.9kJmol-1,4Al(s) + 2O3(g) ═ 2A12O3(s) △H = -3119.1kJmol-1,则O2比O3稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Fe3+和I-在水溶液中的反应为2I-+2Fe3+![]() I2+2Fe2+。某温度下该反应的正反应速率和I-、Fe3+浓度的关系为v=kcm(I-)·cn(Fe3+)(k为常数)。
I2+2Fe2+。某温度下该反应的正反应速率和I-、Fe3+浓度的关系为v=kcm(I-)·cn(Fe3+)(k为常数)。
c(I-)/mol·L-1 | c(Fe3+)/mol·L-1 | v/mol·L-1·s-1 | |
① | 0.20 | 0.80 | 0.032k |
② | 0.60 | 0.40 | 0.144k |
③ | 0.80 | 0.20 | 0.128k |
由此推知,有关Fe3+、I-的浓度对反应速率影响的判断正确的是 ( )
A. Fe3+浓度对正反应速率的影响程度大于I-浓度的影响程度
B. Fe3+浓度对正反应速率的影响程度小于I-浓度的影响程度
C. Fe3+浓度对正反应速率的影响程度等于I-浓度的影响程度
D. 无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O)具有良好的热稳定性、耐热性、电绝缘性,是目前用量最大的热稳定剂,工业上利用铅废渣(主要含PbSO4、 PbCl2、 SiO2)制取三盐基硫酸铅及PbO2工艺流程如下:

已知:①“浸出”过程发生的反应:PbSO4(s)+2Cl-(aq)![]() PbCl2+SO42-(aq)和
PbCl2+SO42-(aq)和
PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0,
PbCl42-(aq) △H>0,
②Ksp(PbCl2)=1.7×10-5 Ksp(PbSO4)=2.5×10-8
回答下列问题:
(1)铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和___________。
(2)“操作1”通过多步操作得到PbCl2,分别为___________、___________、过滤、洗涤。
(3)“转化”后得到PbSO4,当c(Cl-)=0.100mol/L时,c(SO42-)=___________(结果保留一位小数);“转化”时需要升高体系温度,其原因是_________________________________。
(4)写出合成三盐基硫酸铅的化学方程式_________________________________。
(5)氨水络合后铅的存在形态是[ Pb(OH)SO4]-,写出“氧化”发生的离子反应方程式__________________________________________________________________。
(6)一种新型的铅锂电池的充放电示意图如下,写出放电时的正极反应式___________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的混合气体在密闭容器中发生反应:mA(g)+nB(g)![]() pC(g)。达到平衡时,维持温度不变,将气体体积缩小到原来的1/2,当达到新的平衡时,气体C的浓度变为原平衡时的1.9倍。则下列说法正确的是( )
pC(g)。达到平衡时,维持温度不变,将气体体积缩小到原来的1/2,当达到新的平衡时,气体C的浓度变为原平衡时的1.9倍。则下列说法正确的是( )
A. m+n>pB. m+n<p
C. 平衡向正反应方向移动D. C的质量分数增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温、恒容的密闭容器中发生反应A(s)+2B(g)![]() C(g)+D(g),当下列物理量不再变化时,不能够表明该反应已达平衡状态的是
C(g)+D(g),当下列物理量不再变化时,不能够表明该反应已达平衡状态的是
A.混合气体的压强B.混合气体的平均相对分子质量
C.A的物质的量D.B的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图示的分析中,不正确的是

A.如果该图为组成活细胞中的元素,则A是氧元素
B.如果该图表示的是组成细胞的化合物,则A是蛋白质
C.如果该图表示的是活细胞中的元素,则其中Mo的含量很少
D.如果该图为组成细胞的有机化合物,则A中肯定含有的元素为C、H、O、N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种广谱镇痛药,在实验室中合成路线如下(部分反应条件和产物已略去)

(1)A的名称为___________(用系统命名法命名)
(2)由B生成C及由C生成D的反应类型分别为___________、___________。
(3)E的结构简式为______________________。
(4)写出F与NaOH溶液反应的化学方程式_________________________________。
(5)R是G的同分异构体,已知R能与碳酸氢钠溶液反应放出二氧化碳,苯环上有三个取代基,核磁共振氢谱中峰的面积之比为12:2:2:1:1,写出符合条件的两种R的结构简式____________________________________________。
(6)参照上述合成路线,以苯、甲醇和乳酸(![]() )为原料设计合成
)为原料设计合成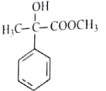 (其它无机试剂任选)。_____________________________________
(其它无机试剂任选)。_____________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com