
【题目】一定温度下,某一密闭且体积不变的容器内有可逆反应:A(g)+2B(g) ![]() 2C(g)。该反应进行到一定限度后达到了化学平衡,不能作为判断该化学平衡标志的是
2C(g)。该反应进行到一定限度后达到了化学平衡,不能作为判断该化学平衡标志的是
A.容器内气体A的物质的量不再随时间而改变
B.容器内气体C的浓度不再随时间而改变
C.单位时间内生成amol物质A,同时生成2amol物质B
D.单位时间内生成amol物质A,同时生成2amol物质C
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
【题目】秸秆(含多糖类物质)的综合利用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:
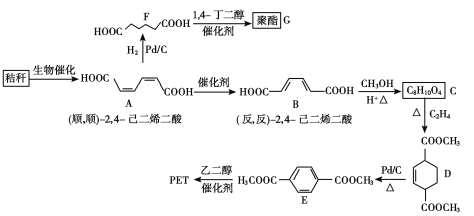
回答下列问题:
(1)下列关于糖类的说法正确的是________。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为________。
(3)D中的官能团名称为________,D生成E的反应类型为________。
(4)F的化学名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示。关于该装置,下列说法正确的是( )
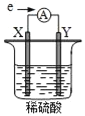
A.外电路中电流方向为:X→![]() →Y
→Y
B.若两电极分别为铁棒和碳棒,则X为碳棒,Y为铁棒
C.X极上发生的是还原反应,Y极上发生的是氧化反应
D.若两电极都是金属单质,则它们的活动性顺序为X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、某实验小组同学进行如下实验,以检验化学反应中的能量变化。请回答下列问题:

(1)实验中发现,反应后①中的温度升高;②中的温度降低.由此判断铝条与盐酸的反应是________,Ba(OH)28H2O与NH4Cl的反应是________.反应过程________(填“①”或“②”)的能量变化可用图2表示。
(2)现有如下两个反应:A、NaOH+HCl=NaCl+H2O;B、2FeCl3+Cu=2FeCl2+CuCl2,以上两个反应能设计成原电池的是________,负极材料为:________,电解质溶液为:________,负极的电极反应式为:________。
Ⅱ、某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。利用如图装置可验证同主族元素非金属性的变化规律
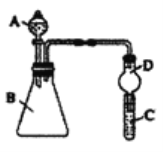
(1)仪器A的名称为________,干燥管D的作用为________。
(2)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液________(填现象)即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用NaOH溶液吸收尾气。
(3)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中可加________溶液,观察到C中溶液________(填现象),即可证明,反应的离子方程式为:________,但有的同学认为该实验不严谨,应在两装置间添加装有________溶液的洗气瓶,目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞香素具有消炎杀菌作用,结构如图所示,下列叙述正确的是
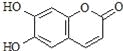
A.与稀H2SO4混合加热不反应
B.不能使酸性高锰酸钾溶液褪色
C.1mol 瑞香素最多能与3mol Br2发生反应
D.1mol瑞香素与足量的NaOH溶液发生反应时,消耗NaOH 3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】14C是一种放射性同位素,在高层大气中由宇宙射线产生的中子或核爆炸产生的中子轰击14N可使它转变为14C。下列就法正确的是( )
A.14C和14N互为同位素B.14C和14N具有相同的质子数
C.![]() 核素中的中子数为8D.14CO2的摩尔质量为46
核素中的中子数为8D.14CO2的摩尔质量为46
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷是一种用于抑制血小板聚集的药物,合成线路如图:
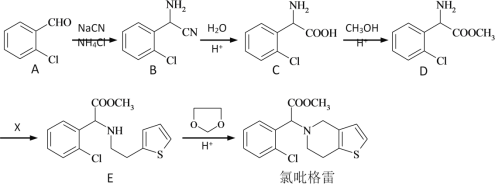
(1)C→D的反应类型____,X的化学式是(C6H7BrS),X的结构简式___。
(2)写出C聚合成高分子化合物的结构简式___。
(3)E合成氯吡格雷的反应中,另一个有机产物的结构简式___。
(4)物质A的同系物G,比A多一个碳原子且苯环上一溴代物只有两种的可能结构有___种。
(5)已知①同一个碳原子上连有两个羟基是不稳定的,极易脱水转变为![]() ,②
,②![]() 中氯原子在水溶液中不水解,写出2-氯甲苯(
中氯原子在水溶液中不水解,写出2-氯甲苯( )经两步反应合成A的化学方程式。____,合成A时产生的有机副产物可能是____。
)经两步反应合成A的化学方程式。____,合成A时产生的有机副产物可能是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法正确的是( )
A.1mol苯乙烯中含有的![]() 键数为4NA
键数为4NA
B.2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C.0.1molCnH2n+2中含有的C—C键数为0.1nNA
D.标准状况下,2.24LCCl4中含有的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,A元素是地壳中含量最多的金属元素;B元素的原子其M层电子数比L层少1个电子;C元素的原子得到2个电子,D元素的原子失去1个电子,所得到的微粒都具有与氩原子相同的电子数,回答下列问题:
(1)上述四种元素的名称分别是A___________,B___________,C____________,D____________,
(2)画出A离子、C原子的结构示意图_____________________,__________________。
(3)写出D与水反应离子方程式______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com