
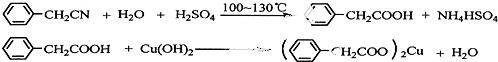
·ÖĪö £Ø1£©ÅäÖĘ“ĖĮņĖįŹ±£¬Ó¦½«ĆܶȓóµÄ×¢ČėĆܶȊ”µÄŅŗĢåÖŠ£¬·ĄÖ¹»ģŗĻŹ±·Å³öČČŹ¹ŅŗµĪ·É½¦£»
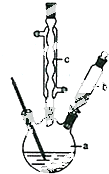
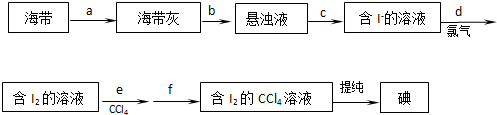
£Ø2£©ÓÉĶ¼æÉÖŖ£¬cĪŖĄäÄż¹Ü£¬Ź¹Ęų»ÆµÄŅŗĢåĄäÄż»ŲĮ÷£¬ŅĒĘ÷bæɼÓČė·“Ó¦Ņŗ£»·“Ó¦½įŹųŗó¼ÓŹŹĮæĄäĖ®£¬½µµĶĪĀ¶Č£¬¼õŠ”±½ŅŅĖįµÄČܽā¶Č£»·ÖĄė±½ŅŅĖį“ÖĘ·£¬ĄūÓĆ¹żĀĖ²Ł×÷£»
£Ø3£©±½ŅŅĖįĪ¢ČÜÓŚĄäĖ®£¬ŌŚĖ®ÖŠµÄČܽā¶Č½ĻŠ”£»ÓÉ·“Ó¦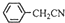 +H2O+H2SO4 $\stackrel{100-130”ę}{”ś}$
+H2O+H2SO4 $\stackrel{100-130”ę}{”ś}$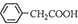 +NH4HSO4æÉÖŖ£¬40g±½ŅŅėęÉś³É±½ŅŅĖįĪŖ40g”Į$\frac{136}{117}$=46.5g£»
+NH4HSO4æÉÖŖ£¬40g±½ŅŅėęÉś³É±½ŅŅĖįĪŖ40g”Į$\frac{136}{117}$=46.5g£»
£Ø4£©ÓĆÕōĮóĖ®Ļ“µÓ³Įµķ£¬½«ĀČĄė×ÓĻ“µÓøɾ»£¬ĄūÓĆĻõĖįŅų¼ģŃéĻ“µÓŅŗČ·¶ØŹĒ·ńĻ“µÓøɾ»£»
£Ø5£©±½ŅŅĖįĪ¢ČÜÓŚĄäĖ®£¬ČÜÓŚŅŅ“¼£¬»ģŗĻČܼĮÖŠŅŅ“¼æÉŌö“ó±½ŅŅĖįµÄČܽā¶Č£®
½ā“š ½ā£ŗ£Ø1£©Ļ”ŹĶÅØĮņĖį·Å³ö“óĮæµÄČČ£¬ÅäÖĘ“ĖĮņĖįŹ±£¬Ó¦½«ĆܶȓóµÄ×¢ČėĆܶȊ”µÄŅŗĢåÖŠ£¬·ĄÖ¹»ģŗĻŹ±·Å³öČČŹ¹ŅŗµĪ·É½¦£¬Ōņ¼ÓČėÕōĮóĖ®ÓėÅØĮņĖįµÄĻČŗóĖ³ŠņŹĒĻČ¼ÓĖ®”¢ŌŁ¼ÓČėÅØĮņĖį£¬
¹Ź“š°øĪŖ£ŗĻČ¼ÓĖ®”¢ŌŁ¼ÓČėÅØĮņĖį£»
£Ø2£©ÓÉĶ¼æÉÖŖ£¬cĪŖĒņŠĪĄäÄż¹Ü£¬Ęä×÷ÓĆĪŖ»ŲĮ÷£Ø»ņŹ¹Ęų»ÆµÄ·“Ó¦ŅŗĄäÄż£©£¬ŅĒĘ÷bµÄ×÷ÓĆĪŖµĪ¼Ó±½ŅŅėę£»·“Ó¦½įŹųŗó¼ÓŹŹĮæĄäĖ®£¬½µµĶĪĀ¶Č£¬¼õŠ”±½ŅŅĖįµÄČܽā¶Č£¬Ōņ¼ÓČėĄäĖ®æɱćÓŚ±½ŅŅĖįĪö³ö£»·ÖĄė±½ŅŅĖį“ÖĘ·£¬ĄūÓĆ¹żĀĖ²Ł×÷£¬ŌņŠčŅŖµÄŅĒĘ÷ĪŖĀ©¶·”¢ÉÕ±”¢²£Į§°ō£¬
¹Ź“š°øĪŖ£ŗµĪ¼Ó±½ŅŅėę£»ĒņŠĪĄäÄż¹Ü£»»ŲĮ÷£Ø»ņŹ¹Ęų»ÆµÄ·“Ó¦ŅŗĄäÄż£©£»±ćÓŚ±½ŅŅĖįĪö³ö£»BCE£»
£Ø3£©±½ŅŅĖįĪ¢ČÜÓŚĄäĖ®£¬ŌŚĖ®ÖŠµÄČܽā¶Č½ĻŠ”£¬ŌņĢį“æ±½ŅŅĖįµÄ·½·ØŹĒÖŲ½į¾§£»ÓÉ·“Ó¦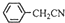 +H2O+H2SO4 $\stackrel{100-130”ę}{”ś}$
+H2O+H2SO4 $\stackrel{100-130”ę}{”ś}$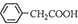 +NH4HSO4æÉÖŖ£¬40g±½ŅŅėęÉś³É±½ŅŅĖįĪŖ40g”Į$\frac{136}{117}$=46.5g£¬×īÖÕµĆµ½44g“æĘ·£¬Ōņ±½ŅŅĖįµÄ²śĀŹŹĒ $\frac{44g}{46.5g}$”Į100%=95%£¬
+NH4HSO4æÉÖŖ£¬40g±½ŅŅėęÉś³É±½ŅŅĖįĪŖ40g”Į$\frac{136}{117}$=46.5g£¬×īÖÕµĆµ½44g“æĘ·£¬Ōņ±½ŅŅĖįµÄ²śĀŹŹĒ $\frac{44g}{46.5g}$”Į100%=95%£¬
¹Ź“š°øĪŖ£ŗÖŲ½į¾§£»95%£»
£Ø4£©ÓĆÕōĮóĖ®Ļ“µÓ³Įµķ£¬½«ĀČĄė×ÓĻ“µÓøɾ»£¬ĄūÓĆĻõĖįŅų¼ģŃéĻ“µÓŅŗČ·¶ØŹĒ·ńĻ“µÓøɾ»£¬Ōņ³ĮµķĻ“øɾ»µÄŹµŃé²Ł×÷ŗĶĻÖĻóŹĒČ”×īŗóŅ»“ĪÉŁĮæĻ“µÓŅŗ£¬¼ÓČėĻ”ĻõĖį£¬ŌŁ¼ÓČėAgNO3ČÜŅŗ£¬ĪŽ°×É«»ė×Ē³öĻÖ£¬
¹Ź“š°øĪŖ£ŗČ”×īŗóŅ»“ĪÉŁĮæĻ“µÓŅŗ£¬¼ÓČėĻ”ĻõĖį£¬ŌŁ¼ÓČėAgNO3ČÜŅŗ£¬ĪŽ°×É«»ė×Ē³öĻÖ£»
£Ø5£©±½ŅŅĖįĪ¢ČÜÓŚĄäĖ®£¬ČÜÓŚŅŅ“¼£¬»ģŗĻČܼĮÖŠŅŅ“¼æÉŌö“ó±½ŅŅĖįµÄČܽā¶Č£¬Č»ŗóÓėCu£ØOH£©2·“Ó¦³żČ„±½ŅŅĖį£¬¼“»ģŗĻČܼĮÖŠŅŅ“¼µÄ×÷ÓĆŹĒŌö“ó±½ŅŅĖįČܽā¶Č£¬±ćÓŚ³ä·Ö·“Ó¦£¬¹Ź“š°øĪŖ£ŗŌö“ó±½ŅŅĖįČܽā¶Č£¬±ćÓŚ³ä·Ö·“Ó¦£®
µćĘĄ ±¾ĢāĪŖ2014Äź¹ćĪ÷øßæ¼»ÆѧŹŌĢā£¬²ąÖŲĪļÖŹÖʱøŹµŃé¼°ÓŠ»śĪļŠŌÖŹµÄ漲飬°ŃĪÕŗĻ³É·“Ó¦¼°ŹµŃé×°ÖƵÄ×÷ÓĆĪŖ½ā“šµÄ¹Ų¼ü£¬×ŪŗĻæ¼²éѧɜŹµŃé¼¼ÄÜŗĶ·ÖĪö½ā“šĪŹĢāµÄÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāŠÅĻ¢µÄ“¦Ąķ¼°Ó¦ÓĆ£®


 ×Ö“Ź¾äĘŖÓėĶ¬²½×÷ĪÄ“ļ±źĻµĮŠ“š°ø
×Ö“Ź¾äĘŖÓėĶ¬²½×÷ĪÄ“ļ±źĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢĄÄ·Éś | B£® | ²£¶ū | C£® | Ā¬ÉŖø£ | D£® | ĘÕĄŹæĖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©ŗĶ¼×Ķ鶼ÄÜ·¢Éś¼Ó³É·“Ó¦ | |
| B£® | Ćŗ½¹ÓĶ”¢ŹÆÓĶ”¢»ØÉśÓĶ¶¼ŹōÓŚĢž | |
| C£® | ¼×Ķ锢ŅŅĻ©”¢±½¶¼æÉĶعżŹÆÓĶ·ÖĮóµĆµ½ | |
| D£® |  + +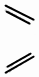 $\stackrel{”÷}{”ś}$ $\stackrel{”÷}{”ś}$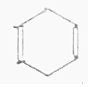 ·“Ó¦ŹōÓŚ¼Ó³É·“Ó¦ ·“Ó¦ŹōÓŚ¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| Ź±¼ä£Øs£© | 0 | 1 | 2 | 3 | 4 | 5 |
| n£ØNO£©£Ømol£© | 0.020 | 0.010 | 0.009 | 0.008 | 0.008 | 0.008 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĘųĢåµÄĆܶȷ¢ÉśĮĖ±ä»Æ | B£® | ĘųĢåµÄĘ½¾ł·Ö×ÓĮæ·¢ÉśĮĖ±ä»Æ | ||
| C£® | ĘųĢåµÄŃÕÉ«·¢ÉśĮĖ±ä»Æ | D£® | ĢåĻµµÄĪĀ¶Č·¢ÉśĮĖ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 µē×ÓĢģĘ½ b£®
µē×ÓĢģĘ½ b£® ŪįŪö c£®
ŪįŪö c£® øÉŌļĘ÷ d£®
øÉŌļĘ÷ d£® ¾Ę¾«ÅēµĘ
¾Ę¾«ÅēµĘ| ¼ÓČČĒ°ÖŹĮæ | ¼ÓČČŗóÖŹĮæ | |
| m1£ØČŻĘ÷£© | m2£ØČŻĘ÷+¾§Ģ壩 | m3£ØČŻĘ÷+ĪŽĖ®ĮņĖįĶ£© |
| 5.200g | 7.900g | 6.900g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
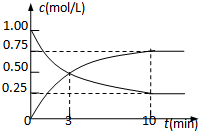 ĪŖŹµĻÖ”°½ŚÄܼõÅÅ”±ŗĶ”°µĶĢ¼¾¼Ć”±µÄŅ»ĻīæĪĢāŹĒČēŗĪ½«CO2×Ŗ»ÆĪŖæÉĄūÓĆ׏Ō“£®ÄæĒ°£¬¹¤ŅµÉĻ³£ÓĆCO2Ą“Éś²śČ¼ĮĻ¼×“¼£®ĻÖ½ųŠŠČēĻĀŹµŃé£ŗŌŚĢå»żĪŖl LµÄĆܱÕŗćČŻČŻĘ÷ÖŠ£¬³äČėl mol CO2ŗĶ3mol H2£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗ
ĪŖŹµĻÖ”°½ŚÄܼõÅÅ”±ŗĶ”°µĶĢ¼¾¼Ć”±µÄŅ»ĻīæĪĢāŹĒČēŗĪ½«CO2×Ŗ»ÆĪŖæÉĄūÓĆ׏Ō“£®ÄæĒ°£¬¹¤ŅµÉĻ³£ÓĆCO2Ą“Éś²śČ¼ĮĻ¼×“¼£®ĻÖ½ųŠŠČēĻĀŹµŃé£ŗŌŚĢå»żĪŖl LµÄĆܱÕŗćČŻČŻĘ÷ÖŠ£¬³äČėl mol CO2ŗĶ3mol H2£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
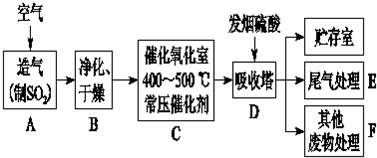
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com