
【题目】通过你的观察和推理,判断下列实验室中对于少量Na的保存方法正确的是 ( )
A. 保存在水中 B. 密封,保存在广口瓶中
C. 用铝箔包裹,密封在广口瓶中 D. 密封,保存在煤油中
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有0.5mol的Y元素的离子得到6.02×1023个电子后被还原成中性Y原子,另外已知0.4gY的氧化物恰好与100mL 0.2molL﹣1 的盐酸完全反应,且Y原子核内质子数和中子数相等.若Y是短周期中某种金属元素.回答下列问题:
(1)Y的名称为 , 它在周期表的位置为;
(2)Y的氧化物与盐酸反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可用于实验室制备二氧化碳的药品是( )
A. KClO3与MnO2的加热 B. Zn、稀H2SO4
C. 浓盐酸、MnO2 D. CaCO3 、盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,22.4 L庚烷的分子数约为NA
B. 1 L 0.1 mol·L-l的Na2S溶液中S2-和HS-的总数为0.1NA
C. 4.0 g H![]() O与D2O的混合物中所含中子数为2NA
O与D2O的混合物中所含中子数为2NA
D. 50 mL 12 mol·L-1盐酸与足量MnO2共热,转移的电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一碳化学”是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学。发展“一碳化学”,开发利用我国相对丰富的煤炭资源具有重要的战略意义和经济价值。下面是以焦炭为原料,经“一碳化学”途径制取乙二醇的过程:
(1)在容积为2L的密闭容器中,由CO和H2合成乙醇的反应为
2CO(g)+ 4H2(g)![]() CH3CH2OH(g)+ H2O(g),在其他条件不变的情况下,CO的转化率随温度的变化如图所示(注:T1、T2均大于280℃):
CH3CH2OH(g)+ H2O(g),在其他条件不变的情况下,CO的转化率随温度的变化如图所示(注:T1、T2均大于280℃):
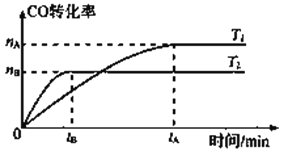
①根据上图可推知该反应ΔH_________0(填“>”、“<”或“=”)。
②该反应的平衡常数表达式为____________,降低温度平衡常数将_____(填“变大”、“变小”或“不变”)。
③下列说法中能判断该反应达到化学平衡状态的是_________(选填编号)。
a.容器中的压强不变 b.混合气体的密度不再变化
c.v正(CO)=2v逆(H2O) d.混合气体的平均相对分子质量不再变化
(2)草酸二甲酯水解产物草酸(H2C2O4)为二元中强酸
①用离子方程式解释KHC2O4溶液显酸性的原因:_______________。
②向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是________(填序号)。
a.c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-)
b.c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-)
c.c(Na+)=c(H2C2O4)+c(C2O42-)
d.c(K+)>c(Na+)
(3)CH3OH(l)气化时吸收的热量为27kJ/mol,CH3OH(g)的燃烧热为677kJ/mol,请写出CH3OH(l)完全燃烧的热化学方程式______________________________。以甲醇为原料,使用酸性电解质构成燃料电池,该燃料电池的负极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,合成氨的反应N2+3H2![]() 2NH3,现将2mol N2和2mol H2通入该容器中反应,20s后生成0.8 mol的NH3,则H2的转换率是多少( )
2NH3,现将2mol N2和2mol H2通入该容器中反应,20s后生成0.8 mol的NH3,则H2的转换率是多少( )
A. 70% B. 60% C. 50% D. 40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生的实验报告所列出的下列数据中合理的是( )
A.用10mL量筒量取7.13mL稀盐酸B.用pH计测得某稀盐酸的pH为1.54
C.用25mL碱式滴定管量取出15.00mLKMnO4溶液D.用托盘天平称得某物质的质量为13.15g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=______.
已知:K1000℃>K800℃,则该反应是_________反应。(填“吸热”或“放热”);
(2)已知在800 ℃时,该反应的平衡常数K1=0.9,则该温度下反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数K2 = ______________ ,反应CO2(g)+H2(g)
CO2(g)+H2(g)的平衡常数K2 = ______________ ,反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的平衡常数K3 =_______________ 。
CO(g)+H2O(g)的平衡常数K3 =_______________ 。
(3)能判断该反应是否达到化学平衡状态的依据是_____________。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(H2)=c(CO)c(H2O),试判断此时的温度为_____________℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读图,下列判断不正确的是
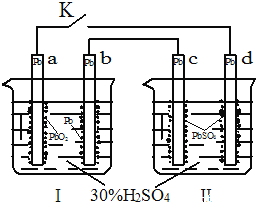
A. K闭合时,d电极反应式:PbSO4+2H2O-2e-═PbO2+4H++SO42-
B. 当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2mol
C. K闭合时,II中SO42-向c电极迁移
D. K闭合一段时间后,II可单独作为原电池,d电极为正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com