
| A.残余固体可能为铁、铜混合物 | B.最后得到的溶液中含有Fe3+ |
| C.最后得到的溶液中只含Cu2+ | D.残余固体一定全部是铜 |
 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.该晶体中没有SCN- | B.Fe3+的氧化性比Cl2的氧化性强 |
| C.Fe2+被Cl2氧化为Fe3+ | D.Fe2+与SCN-形成血红色的化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
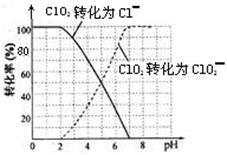
 ,工业上用湿法制备高铁酸钾的基本流程如下图所示:
,工业上用湿法制备高铁酸钾的基本流程如下图所示: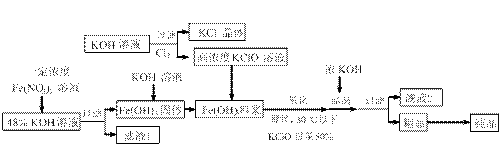
 。
。
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.8g | B.0.8ag | C.(a—1.6)g | D.(a—0.8)g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入HNO3将Fe2+氧化成Fe3+,再加水稀释至pH4-5 |
| B.向溶液中通入Cl2,再加入CuO粉末调节至pH4-5 |
| C.向溶液中通入Cl2,在通入NH3调节至pH4-5 |
| D.向溶液中通入H2O2, 再加入CuO粉末调节至pH4-5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.消耗硫酸亚铁铵的物质量为n(2-x)mol |
| B.处理废水中Cr2O72-的物质量为mol |
| C.反应中发生转移的电子数为3nx mol |
| D.在FeO·FeyCrxO3中3x=y |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com