
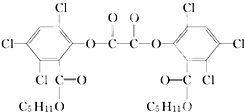
 夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )
夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )| A、草酸二酯的分子式为C26H24Cl6O8 |
| B、1 mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4 mol NaOH |
| C、该有机物能发生加成反应、取代反应、氧化反应 |
| D、1 mol草酸二酯与氢气完全反应,需要氢气6 mol |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
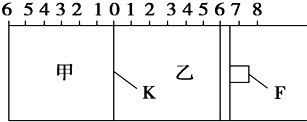
| A、石蕊层仍为紫色 |
| B、石蕊层有两层,上层为紫色,下层为蓝色 |
| C、石蕊层为三层环,由上而下是蓝色、紫色、红色 |
| D、石蕊层为三层环,由上而下是红色、紫色、蓝色. |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某有机物的结构简式如图,关于该物质的下列说法:①能和溴水发生取代反应 ②能发生消去反应 ③能发生氧化反应 ④能发生加成反应 ⑤能发生水解反应,其中不正确的是( )
某有机物的结构简式如图,关于该物质的下列说法:①能和溴水发生取代反应 ②能发生消去反应 ③能发生氧化反应 ④能发生加成反应 ⑤能发生水解反应,其中不正确的是( )| A、①③ | B、②⑤ | C、②③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com