
下列电离或水解方程式正确的是
A.Na2SO3的水解:SO32-+ 2H2O H2SO3 + 2OH-
H2SO3 + 2OH-
B.NaHCO3的电离:NaHCO3  Na + + H+ + CO32-
Na + + H+ + CO32-
C.KHS的电离:HS- + H2O  H3O+ + S2-
H3O+ + S2-
D.NaClO溶液与FeCl2溶液混合:2ClO- + Fe2+ + 2H2O = 2HClO + Fe(OH)2↓
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A.锌片插入硝酸银溶液中Zn+Ag+===Zn2++Ag
B.碳酸氢钙溶液加到醋酸中
Ca(HCO3)2+2CH3COOH===Ca2++2CH3COO-+2CO2↑+2H2O
C.少量金属钠加到冷水中
Na+2H2O===Na++OH-+H2↑
D.氢氧化铜加到盐酸中
Cu(OH)2+2H+===Cu2++2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
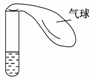
某学生课外活动小组利用右图所示装置分别进行如下实验:
(1)向试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是______________溶液;加热时溶液由红色逐渐变浅的原因是_______________。
(2)向试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则原溶液可能是____________________溶液;加热时溶液由无色变为红色的原因是_____________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某反应2AB(g)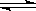 C(g)+ 3D (g)在高温下能自发进行,其逆反应在低温下能自发进行,则该反应的ΔH、ΔS应为
C(g)+ 3D (g)在高温下能自发进行,其逆反应在低温下能自发进行,则该反应的ΔH、ΔS应为
A.ΔH <0,ΔS>0 B.ΔH <0,ΔS<0 C.ΔH >0,ΔS>0 D.ΔH >0,ΔS<0
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为: 3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述不正确的是
A.放电时负极反应为:3Zn-6e-+6OH-====3Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH- FeO42- +4H2O
FeO42- +4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被还原
D.充电时阴极溶液的碱性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸是重要的化工原料,二氧化硫生成三氧化硫是硫酸工业的重要反应之一。
(1)将0.100 mol SO2(g)和0.060 mol O2(g)放入容积为2 L的密闭容器中,反应2SO2(g)+O2(g)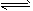 2SO3(g)在一定条件下5分钟末达平衡状态,测得c(SO3)=0.040 mol/L。
2SO3(g)在一定条件下5分钟末达平衡状态,测得c(SO3)=0.040 mol/L。
①从平衡角度分析采用过量O2的目的是____ ▲ ____;
②列式并计算该条件下反应的平衡常数K=____ ▲ ____。
③已知:K(300℃)>K(350℃),若反应温度升高,SO2的转化率____ ▲ ____(填“增大”、“减小”或“不变”)。
④能判断该反应达到平衡状态的标志是____ ▲ ____。(填字母)
A.SO2和SO3浓度相等 B.容器中混合气体的平均分子量保持不变
C.容器中气体的压强不变 D.SO3的生成速率与SO2的消耗速率相等。
(2)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如下图1所示。平衡状态由A变到B时,平衡常数K(A)___ ▲ ____K(B)(填“>”、“<”或“=”)。
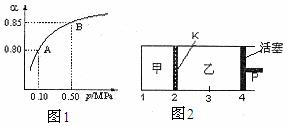
(3)如图2所示,保持温度不变,在一定反 应条件下,将2molSO2和1molO2加入甲容器中,将4molSO2和2molO2加入乙容器中,隔板K不能移动。此时控制活塞P,使乙的容积为甲的2倍。
①若移动活塞P,使乙的容积和甲相等,达到新平衡时,SO3的体积分数甲_ ▲ 乙。(填:“大于”、“小于”、或“等于”)
②若在甲容器中通入一定量的He气,使容器内的压强增大,则c(SO3)/c(SO2)将__ _ ▲ ____填:“增大”、“减小”、“不变”、“无法确定”)
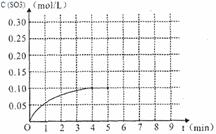 (4)将一定量的SO2(g)和O2(g)放入某固定体积的密闭容器中,在一定条件下,c(SO3)的变化如下图所示。若在第5分钟将容器的体积缩小一半后,在第8分钟达到新的平衡(此时SO3的浓度约为0.25mol/L)。请在下图中画出此变化过程中SO3浓度的变化曲线。
(4)将一定量的SO2(g)和O2(g)放入某固定体积的密闭容器中,在一定条件下,c(SO3)的变化如下图所示。若在第5分钟将容器的体积缩小一半后,在第8分钟达到新的平衡(此时SO3的浓度约为0.25mol/L)。请在下图中画出此变化过程中SO3浓度的变化曲线。
查看答案和解析>>
科目:高中化学 来源: 题型:
用36.5%的浓盐酸(密度1.2 g·cm-3)配1 mol·L-1的稀盐酸 100 mL,配制过程所用仪器,且使用先后顺序正确的是
①100 mL量筒 ②10 mL量筒 ③50 mL 烧杯 ④电子天平 ⑤100 mL容量瓶
⑥胶头滴管 ⑦玻璃棒
A.①③⑤⑥⑦ B.②③⑦⑤⑥ C.③⑤⑦⑥① D.④③⑦⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,氯元素被氧化的是
A.2KClO3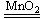 2KCl+3O2↑ B.2P+5Cl2
2KCl+3O2↑ B.2P+5Cl2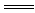 2PCl5
2PCl5
C.MnO2+4HCl(浓)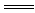 MnCl2十2H2O+Cl2↑ D.H2+Cl2
MnCl2十2H2O+Cl2↑ D.H2+Cl2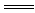 2HCl
2HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com