
 +2[Ag(NH3)2]OH$\stackrel{△}{→}$
+2[Ag(NH3)2]OH$\stackrel{△}{→}$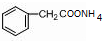 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O. 分析 (1)根据M=$\frac{m}{n}$计算出该有机物的摩尔质量,再根据n=$\frac{m}{M}$计算二氧化碳、水的物质的量,然后根据原子守恒计算分子中C、H原子数目,结合相对分子质量计算分子中O原子数目,据此确定有机物的分子式;
(2)A可以发生银镜反应,含有-CHO,苯环上的一溴代物有三种,苯环上有3种化学环境不同的H原子,结合有机物的分子式书写其结构简式;A发生银镜反应,-CHO被氧化,结合A的结构简式书写反应方程式.
解答 解:(1)0.1mol有机物A的质量是12g,则A的摩尔质量为:$\frac{12g}{0.1mol}$=120g/mol,
0.1molA在足量的氧气中充分燃烧后生成35.2g CO2和7.2g H2O,二氧化碳的物质的量为:$\frac{35.2g}{44g/mol}$=0.8mol,水的物质的量为:$\frac{7.2g}{18g/mol}$=0.4mol,根据原子守恒可知,该有机物中N(C)=$\frac{0.8mol}{0.1mol}$=8、N(H)=$\frac{0.4mol×2}{0.1mol}$=8,故有机物中N(O)=$\frac{120-12×8-8}{16}$=1,故有机物的分子式为C8H8O,
故答案为:C8H8O;
(2)有机物的分子式为C8H8O,A可以发生银镜反应,含有醛基-CHO,苯环上的一溴代物有三种,苯环上有3种化学环境不同的H原子,故只能有1个侧链为-CH2CHO,结构简式为: ,
, 发生银镜反应的化学方程式为:
发生银镜反应的化学方程式为: +2[Ag(NH3)2]OH$\stackrel{△}{→}$
+2[Ag(NH3)2]OH$\stackrel{△}{→}$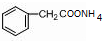 +2Ag↓+3NH3+H2O,
+2Ag↓+3NH3+H2O,
故答案为: +2[Ag(NH3)2]OH$\stackrel{△}{→}$
+2[Ag(NH3)2]OH$\stackrel{△}{→}$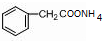 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.
点评 本题考查有机物分子式、结构简式的确定,题目难度中等,明确常见有机物结构与性质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的化学计算能力.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | FeS不溶于水,但能溶于稀盐酸中 | |
| B. | 在氯化氢气流中加热蒸发CuCl2溶液以制备CuCl2•2H2O | |
| C. | 将饱和FeCl3溶液滴入沸水中以制备氢氧化铁胶体 | |
| D. | 实验室配制硫化钾溶液时加入适量KOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
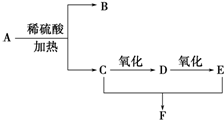
 CH3COOH+CH3OH.
CH3COOH+CH3OH.查看答案和解析>>
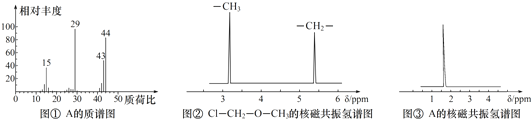
科目:高中化学 来源: 题型:实验题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
| B | 乙醇(乙酸) | KOH溶液 | 分液 |
| C | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| D | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A. | X离子的氧化性比Y离子氧化性强 | |
| B. | 一定条件下,Z单质与W的常见单质直接生成ZW2 | |
| C. | Y的最高价氧化物对应的水化物能溶于氨水 | |
| D. | W单质的氧化性比Z单质强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4mol | B. | 3.4mol | C. | 2.8mol | D. | 1.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能够使甲基橙呈现黄色 | B. | 溶液的pH>7 | ||
| C. | 溶液中:c(H+)>1×10-7mol•L-1 | D. | 溶液中:c(H+)<c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com