
| A. | 滤液A中的溶质主要是NaAlO2和NaOH | |
| B. | 调pH时,可以加入CuO或Cu2(OH)2CO3 | |
| C. | 操作②是在蒸发皿中直接蒸干水分 | |
| D. | 该合金中含有的金属主要为铁、铜、铝 |
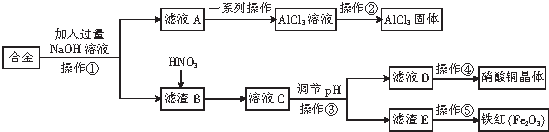
分析 合金加入NaOH溶液后金属铝溶解生成偏铝酸钠溶液,金属铁和金属铜不与氢氧化钠反应,滤液A中含有偏铝酸钠,滤渣B为铁、铜,铜和铁与稀硝酸能发生反应生成硝酸盐和一氧化氮、水,一氧化氮、水、氧气反应生成硝酸再循环利用,溶液C通过调节pH可以使Fe3+沉淀完全,滤渣E为氢氧化铁,滤液D为硝酸铜溶液,用加热浓缩、冷却结晶、过滤、洗涤、干燥的方法得到硝酸铜晶体,灼烧氢氧化铁得到铁红,据此分析.
解答 解:合金加入NaOH溶液后金属铝溶解生成偏铝酸钠溶液,金属铁和金属铜不与氢氧化钠反应,滤液A中含有偏铝酸钠,滤渣B为铁、铜,铜和铁与稀硝酸能发生反应生成硝酸盐和一氧化氮、水,一氧化氮、水、氧气反应生成硝酸再循环利用,溶液C通过调节pH可以使Fe3+沉淀完全,滤渣E为氢氧化铁,滤液D为硝酸铜溶液,用加热浓缩、冷却结晶、过滤、洗涤、干燥的方法得到硝酸铜晶体,灼烧氢氧化铁得到铁红,
A.合金与过量NaOH溶液反应,生成偏铝酸钠,所以滤液A中的溶质主要是NaAlO2和NaOH,故A正确;
B.调节pH时不能引入新的杂质,可知可以加入CuO或Cu2(OH)2CO3,故B正确;
C.氯化铝溶液在HCl气氛中加热可以得到无水氯化铝,若直接加热会水解生成氢氧化铝沉淀,故C错误;
D.合金制得氯化铝固体、硝酸铜晶体和铁红,由元素守恒可知,该合金中含有的金属主要为铁、铜、铝,故D正确.
故选C.
点评 本题考查了物质的制备、物质分离提纯操作实验,题目综合性较强,要注意从框图转化中找出有用信息,题目难度中等,侧重于考查学生的分析能力和对基础知识的应用能力.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 |  |  |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌锰干电池电极总反应为:Zn+2MnO2+2NH4Cl=Mn2O3+ZnCl2+2NH3+H2O,则正极反应为:2MnO2+2H++2e-=Mn2O3+H2O | |
| B. | 将1mol过氧化钠投入含有1molAlCl3的溶液中:6Na2O2+6H2O+4Al3+=4Al(OH)3↓+3O2↑+12Na+ | |
| C. | NaHSO4溶液中加入Ba(OH)2溶液至溶液呈中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 将16.8g 铁粉投入100mL 4.0mol/L的HNO3溶液中(还原产物只有NO)6Fe+20 H++5NO3-=3Fe2++3Fe3++5NO↑+10H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2+2H2O+Cl2═H2SO4+2HCl | B. | SO2+H2S═2H2O+3S | ||
| C. | SO2+2NaOH═Na2SO3+H2O | D. | SO2+Na2CO3═Na2SO3+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | Na2C03溶液显碱性:C032-+H2O═HCO3-+OH- | |
| C. | 过量铁屑溶于稀硝酸:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| D. | FeI2溶液中通入少量氯气:2Fe2++C12═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可燃物在燃烧时所显示的火焰颜色 | |
| B. | 所有元素在灼烧时都有焰色反应 | |
| C. | 多种金属或它们的化合物灼烧时所显示的火焰颜色 | |
| D. | 焰色反应是一种化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、NH4+、Cl-、CO32- | B. | K+、Ba2+、NO3-、HCO3- | ||
| C. | Na+、K+、SO42-、SiO32- | D. | Na+、Cu2+、Br -、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
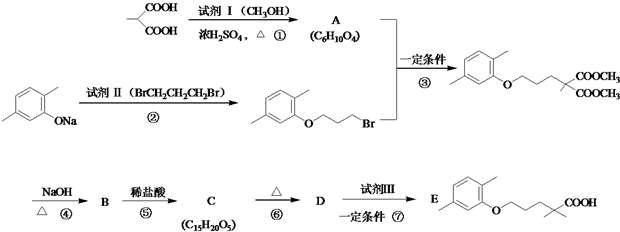
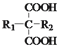 $\stackrel{△}{→}$
$\stackrel{△}{→}$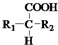 +CO2↑(R1和R2代表烷基)
+CO2↑(R1和R2代表烷基)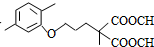 $\stackrel{△}{→}$
$\stackrel{△}{→}$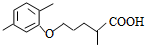 +CO2↑.
+CO2↑.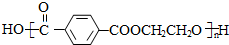 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com