
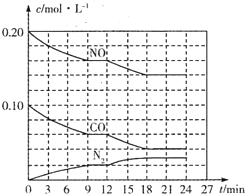
 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.分析 (1)根据v(CO)=$\frac{△c}{△t}$计算CO反应速率;
(2)依据图象分析判断,平衡状态时一氧化碳一氧化氮和氮气浓度,结合化学平衡三段式列式计算平衡百分含量和平衡常数;
(3)计算水解平衡常数Kh,再根据Ka=$\frac{{K}_{w}}{{K}_{h}}$计算.
解答 解:(1)v(CO)=$\frac{△c}{△t}$=$\frac{0.10-0.06}{9}$mol/(L.min)=4.4×10-3mol/(L.min),
故答案为:4.4×10-3;
(2)该反应在第24min时达到平衡状态,平衡浓度c(N2)=0.03mol/L,c(NO)=0.14mol/L,c(CO)=0.04mol/L,依据化学平衡三段式列式计算
2NO(g)+2CO(g)═N2(g)+2CO2(g)
起始量(mol/L) 0.2 0.1 0 0
变化量(mol/L) 0.06 0.06 0.03 0.06
平衡量(mol/L) 0.14 0.04 0.03 0.06
CO2的体积分数=$\frac{0.06}{0.14+0.04+0.03+0.06}$×100%=22.2%
平衡常数K=$\frac{0.0{6}^{2}×0.03}{0.1{4}^{2}×0.0{4}^{2}}$=3.4
故答案为:22.2%;3.4;
(3)常温下,0.1mol/L的HCOONa溶液pH为10,溶液中存在HCOO-水解HCOO-+H2O?HCOOH+OH-,故Kh=$\frac{1{0}^{-4}×1{0}^{-4}}{0.1-1{0}^{-4}}$=10-7,则HCOOH的电离常数Ka=$\frac{{K}_{w}}{{K}_{h}}$=$\frac{1{0}^{-14}}{1{0}^{-7}}$=1×10-7,故答案为:1.0×10-7.
点评 本题考查化学平衡计算、盐类水解平衡计算,为高频考点,侧重考查学生分析计算能力,难点是盐类水解平衡计算,注意弱电解质电离平衡常数与弱离子水解平衡常数关系,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 0.5mol H2O中含有的原子总数为1.5 NA | |
| B. | 0.2mol O2 所占有的体积为4.48L | |
| C. | 22g 二氧化碳气体中所含有的分子数目为0.5 NA | |
| D. | 100mL2mol/L的Na2CO3溶液中含有的Na+数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为相互串联的甲乙两个电解池,甲池若为电解精炼铜的装置,请回答:
如图为相互串联的甲乙两个电解池,甲池若为电解精炼铜的装置,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2的转化率为28.57% | B. | H2的转化率为85.7% | ||
| C. | N2的体积分数为20% | D. | H2的体积分数为10% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| H2O2/% | 5 | 10 | 15 | 20 | 25 | 30 |
| CaO2/% | 62.40 | 63.10 | 63.20 | 64.54 | 62.42 | 60.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、FeCl3、H2SO4 | B. | HCl、K2CO3、BaCl2 | ||
| C. | CuSO4、HCl、KOH | D. | BaCl2、HNO3、AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知C(石墨,s)═C(金刚石,s)△H﹦+1.9kJ•mo1-1,说明金刚石具有的能量比石墨低 | |
| B. | 已知H+(aq)+OH-(aq)═H2O(1)△H﹦-57.4KJ•mo1-1,20g氢氧化钠固体溶于稀盐酸中恰好完全反应时放出的热量大于28.7kJ | |
| C. | 已知甲烷的燃烧热为890.3kJ•mo1-1,则表示甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H﹦-890.3kJ•mo1-1 | |
| D. | 将0.5mo1N2和1.5mo1H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H﹦-38.6kJ•mo1-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com