
【题目】某同学设计如下实验装置用于制取纯净的无水FeCl3.
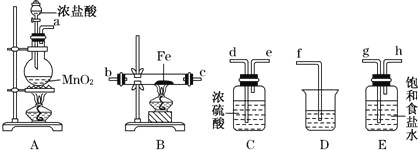
(1)图中盛放浓盐酸的实验仪器的名称为 ,A中发生反应的化学方程式为 .
(2)各装置的正确连接顺序为:a→ → → → → →c→ (填字母代号),
(3)装置E的作用是 ,装置C的作用是 .
(4)装置D中所发生反应的离子方程式为 .
(5)装置A中,如果反应产生氯气的体积为2.24L(标准状况),则反应中被氧化的HCl的质量为 .
【答案】(1)分液漏斗;MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)g;h;d;e;b;f;
(3)除去氯气中的氯化氢;干燥氯气;
(4)Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;
(5)7.3g
【解析】
试题分析:该实验目的是用Cl2和Fe反应制取FeCl3固体,实验室用浓盐酸和MnO2加热制取Cl2,因为要制取纯净干燥的FeCl3,所以生成的Cl2必须是干燥、纯净的,浓盐酸、水都具有挥发性,所以生成的Cl2中含有HCl、H2O,用饱和食盐水除去HCl、用浓硫酸干燥Cl2,氯气有毒,不能直接排空,应该用碱液吸收Cl2;
(1)图中盛放浓盐酸的实验仪器的名称为分液漏斗,实验室用浓盐酸和MnO2加热制取Cl2,二者反应生成氯化锰、氯气和水;
(2)各装置的正确连接顺序为气体制备装置、洗气装置、干燥装置、氯化铁制备装置、尾气处理装置,
(3)装置E的作用是吸收HCl,装置C的作用是干燥气体;
(4)装置D中氯气和碱反应生成氯化物、次氯酸盐和水;
(5)装置A中,如果反应产生氯气的体积为2.24L(标准状况),其物质的量=![]() =0.1mol,根据Cl原子守恒计算反应中被氧化的HCl的物质的量,根据m=nM计算被氧化硫化氢质量.
=0.1mol,根据Cl原子守恒计算反应中被氧化的HCl的物质的量,根据m=nM计算被氧化硫化氢质量.
解:该实验目的是用Cl2和Fe反应制取FeCl3固体,实验室用浓盐酸和MnO2加热制取Cl2,因为要制取纯净干燥的FeCl3,所以生成的Cl2必须是干燥、纯净的,浓盐酸、水都具有挥发性,所以生成的Cl2中含有HCl、H2O,用饱和食盐水除去HCl、用浓硫酸干燥Cl2,氯气有毒,不能直接排空,应该用碱液吸收Cl2;
(1)图中盛放浓盐酸的实验仪器的名称为分液漏斗,实验室用浓盐酸和MnO2加热制取Cl2,二者反应生成氯化锰、氯气和水,反应方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,故答案为:分液漏斗;MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:分液漏斗;MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)各装置的正确连接顺序为气体制备装置、洗气装置、干燥装置、氯化铁制备装置、尾气处理装置,所以其连接顺序是a→g→h→d→e→b→c→f,
故答案为:g;h;d;e;b;f;
(3)装置E的作用是吸收挥发出的HCl,装置C的作用是干燥气体,防止得不到干燥的氯化铁,故答案为:除去氯气中的氯化氢;干燥氯气;
(4)装置D中氯气和碱反应生成氯化物、次氯酸盐和水,离子方程式为Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,故答案为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;
(5)装置A中,如果反应产生氯气的体积为2.24L(标准状况),其物质的量=![]() =0.1mol,根据Cl原子守恒计算反应中被氧化的n(HCl)=2n(Cl2)=2×0.1mol=0.2mol,被氧化m(HCl)=nM=0.2mol×36.5g/mol=7.3g,故答案为:7.3g
=0.1mol,根据Cl原子守恒计算反应中被氧化的n(HCl)=2n(Cl2)=2×0.1mol=0.2mol,被氧化m(HCl)=nM=0.2mol×36.5g/mol=7.3g,故答案为:7.3g


科目:高中化学 来源: 题型:
【题目】如图A是实验室制取二氧化碳并检验其性质的实验装置图,请你回答:
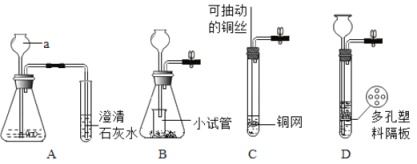
(1)a仪器的名称为______。
(2)写出实验室制取二氧化碳的化学方程式 。
(3)小雨同学按图A方式将导管伸入试管中,溶液未出现浑浊现象,你认为可能的原因是 (答出一条即可)。
(4)为了制取方便,小林同学设计了如图B、C、D三种改进装置,你认为能起到“控制反应的发生和停止”效果的是 (填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护环境日益引起人们的重视。下列做法不利于保护环境的是
A.氢能源代替化石能源
B.推广使用太阳能电池
C.电动汽车代替燃油汽车
D.造纸厂污水直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对化学反应:A(g)+3B(g)═2C(g)+2D(g)来说,下列四种不同情况下的反应速率最快的是( )
A.υ(A)=0.005mol/(Ls)
B.υ(B)=0.6 mol/(Lmin)
C.υ(C)=0.5 mol/(Lmin)
D.υ(D)=0.45 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在200 mL 含Mg2+、Al3+、NH4+、H+、Cl-的溶液中,逐滴加入5 mol·L-1 NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示。下列叙述不正确的是
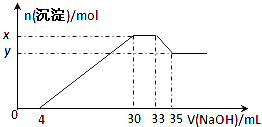
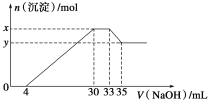 A.x-y=0. 01 mol B.原溶液中c(Cl-)=0.75 mol·L-1
A.x-y=0. 01 mol B.原溶液中c(Cl-)=0.75 mol·L-1
C.原溶液的pH=1 D.原溶液中n(Mg2+)∶n(Al3+)=5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 镁着火不能用CO2灭火
B. 钠只有在加热条件下才能与氯气反应
C. 浓硫酸有氧化性,稀硫酸没有氧化性
D. SO2能使酸性高锰酸钾溶液褪色,说明SO2具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在指定条件下一定能大量共存的是( )
①某无色透明的酸性溶液中:Cl-、Na+、MnO![]() 、SO
、SO![]()
②水电离产生的c(H+)=10-12 mol·L-1的溶液中:K+、Na+、Cl-、NO![]()
③使紫色石蕊溶液变红的溶液中:Fe2+、Mg2+、NO![]() 、Cl-
、Cl-
④加入过量NaOH溶液后可得到澄清溶液:K+、Ba2+、 HCO![]() 、Cl-
、Cl-
⑤c(H+)<c(OH-)的溶液中:SO![]() 、S2-、K+、Na+
、S2-、K+、Na+
⑥在酸性高锰酸钾溶液中:Na+、NH![]() 、I-、ClO-
、I-、ClO-
⑦能使pH试纸变蓝色的溶液中:Na+、AlO![]() 、K+、CO
、K+、CO![]()
A.①③④⑥⑦ B.②③⑤⑦
C.②⑤⑦ D.②④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析不正确的是

A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH-
C.c点,两溶液中含有相同量的OH-
D.a、d两点对应的溶液均显中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com