
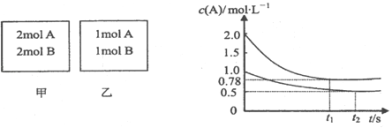
【题目】向甲、乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同温度下,发生反应:A(g)+B(g)xC(g);△H<0.测得两容器中c(A)随时间t的变化如图所示.下列说法正确的是( )
A.x可能等于2
B.甲、乙两容器中反应达平衡时,平衡常数K(甲)<K(乙)
C.将乙容器升温可使甲、乙容器内各物质的体积分数相同
D.若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 molL﹣1<c(A)<1.56 molL﹣1
【答案】D
【解析】
试题分析:由图像可知平衡时,甲容器平衡时,A的转化率为![]() ×100%=61%,乙容器内A的转化率为
×100%=61%,乙容器内A的转化率为![]() ×100%=50%,甲容器内压强比乙容器内大,增大压强向正反应移动,增大压强平衡向着体积减小的方向移动,故:1+1>X,所以x=1。A、由上述分析可知x=1,若x=2,反应前后气体体积不变,甲、乙为等效平衡,转化率相等,A错误;B、平衡常数只与温度有关系,甲、乙两容器中反应达平衡时,平衡常数K(甲)=K(乙),B错误;C、该反应为放热反应,将乙容器单独升温,平衡向吸热反应方向移动,即向逆反应方向移动,A的转化率比甲容器的转化率低,不可能使乙容器内各物质的体积分数与甲容器内的相同,C错误;D、向甲容器中再充入2molA、2molB,可以等效为原平衡状态下压强增大一倍,平衡向正反应方向移动,A转化率增大,所以平衡时甲容器中c(A)小于2倍原平衡中的c(A),平衡移动目的是降低浓度增大趋势,但不能消除浓度增大,达新平衡时浓度比原平衡大,所以平衡时甲容器中0.78mol/L<c(A)<1.56mol/L,D正确,答案选D。
×100%=50%,甲容器内压强比乙容器内大,增大压强向正反应移动,增大压强平衡向着体积减小的方向移动,故:1+1>X,所以x=1。A、由上述分析可知x=1,若x=2,反应前后气体体积不变,甲、乙为等效平衡,转化率相等,A错误;B、平衡常数只与温度有关系,甲、乙两容器中反应达平衡时,平衡常数K(甲)=K(乙),B错误;C、该反应为放热反应,将乙容器单独升温,平衡向吸热反应方向移动,即向逆反应方向移动,A的转化率比甲容器的转化率低,不可能使乙容器内各物质的体积分数与甲容器内的相同,C错误;D、向甲容器中再充入2molA、2molB,可以等效为原平衡状态下压强增大一倍,平衡向正反应方向移动,A转化率增大,所以平衡时甲容器中c(A)小于2倍原平衡中的c(A),平衡移动目的是降低浓度增大趋势,但不能消除浓度增大,达新平衡时浓度比原平衡大,所以平衡时甲容器中0.78mol/L<c(A)<1.56mol/L,D正确,答案选D。


科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是
A. 次氯酸钠溶液可用作环境的杀菌消毒
B. 硅胶可用作商品包装袋的干燥剂
C. 爆竹燃放后,硫燃烧生成SO3
D. 施肥时,草木灰不能与胺态氮肥混合使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
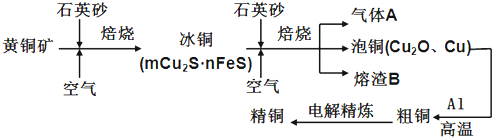
(1)气体A中的大气污染物可选用下列试剂中的 吸收.
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在 (填离子符号),检验溶液中还存在Fe2+的方法是
(3)由泡铜冶炼粗铜的化学反应方程式为 .
(4)取一定量的泡铜,加入1L0.6mol/LHNO3溶液恰好完全溶解,同时放出2240mLNO气体(标准状况),另取等量的泡铜,用足量的H2还原,得到的铜的质量为 g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)某学生研究小组欲探究CuSO4溶液与Na2CO3溶液混合产生的蓝绿色沉淀组成,小组进行下列实验探究。
【提出假设】
假设1:沉淀为Cu(OH)2;假设2:所得沉淀为_____________;
假设3:所得沉淀为碱式碳酸铜[化学式可表示为nCu(OH)2·mCuCO3]。
【查阅资料】无论是哪一种沉淀受热均易分解(假设均不含结晶水)。
【物质成分探究】
步骤1:将所得悬浊液过滤,用蒸馏水洗涤,再用无水乙醇洗涤;
步骤2:甲同学取一定量所得固体,用气密性良好的如图装置(夹持仪器未画出)进行定性实验。
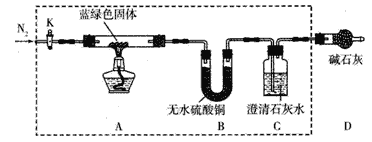
请回答下列问题:
(1)假设2中的沉淀是为______________。
(2)假设1中沉淀为Cu(OH)2的理论依据是_________________。
(3)无水乙醇洗涤的目的__________________。
(4)若反应后A中蓝绿色固体变黑,C中无明显现象,证明假设________________(填写序号)成立。
(5)乙同学认为只要将上图中B装置的试剂改用_______________试剂后,便可验证上述所有假设。
(6)乙同学更换B试剂后验证假设3成立的实验现象是___________________。
(7)在假设3成立的前提下,某同学考虑用Ba(OH)2代替Ca(OH)2,测定蓝绿色固体的化学式,若所取蓝绿色固体质量为27.1g,实验结束后装置B的质量增加2.7g,C中的产生沉淀的质量为19.7g。则该蓝绿色固体的化学式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的应用正确的是
A. 金属钠着火可用泡沫灭火器扑灭
B. 烘焙食品时加入小苏打可以使食品蓬松
C. 氧化亚铁俗称铁红,常用作油漆涂料
D. 用氧化铝制成的坩埚可用于加热苛性钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质结构的说法正确的是( )
A. 电子层数多的原子的半径一定大于电子层数少的原子的半径
B. P4S3分子中各原子的最外层均已达到了8电子稳定结构,则分子中共价键数目为9条
C. H2SO3酸性强于H2CO3,所以非金属性S大于C
D. 不同原子形成的化合物中一定只含极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com