
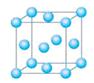
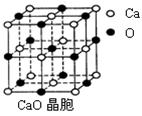
科目:高中化学 来源:不详 题型:单选题
| A.离子晶体中,只存在离子键,不可能存在其它化学键 |
| B.在卤族元素(F、Cl、Br、I)的氢化物中,HF的沸点最低 |
| C.NaHSO4、Na2O2晶体中的阴、阳离子个数比均为1 : 2 |
| D.晶体熔点:金刚石>食盐>冰>干冰 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
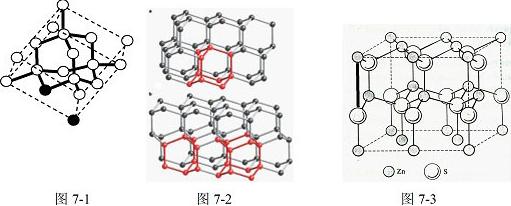
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属原子的核外电子在金属晶体中都是自由电子 |
| B.体心立方晶胞和面心立方晶胞中实际含有的原子个数之比为1:2 |
| C.金属原子在化学变化中失去的电子数越多,其还原性越强 |
| D.金属导电的实质是金属阳离子在外电场作用下的定向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
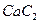 与水反应生成乙炔。
与水反应生成乙炔。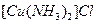 溶液生成
溶液生成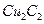 红棕色沉淀。
红棕色沉淀。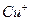 基态核外电子排布式为 。
基态核外电子排布式为 。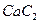 中
中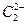 与
与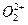 互为等电子体,
互为等电子体,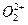 的电子式可表示为 ;1mol
的电子式可表示为 ;1mol 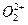 中含有的
中含有的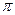 键数目为 。
键数目为 。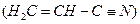 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
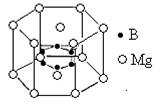
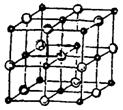
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。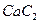 晶体的晶胞结构与
晶体的晶胞结构与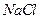 晶体的相似(如下图所示),但
晶体的相似(如下图所示),但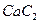 晶体中含有的哑铃形
晶体中含有的哑铃形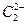 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。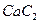 晶体中1个
晶体中1个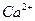 周围距离最近的
周围距离最近的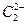 数目为
数目为  。
。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com