
【题目】红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题。
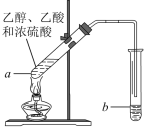
(1) 用化学方法可以鉴别乙醇和乙酸的试剂是______________(填字母);
a.稀硫酸 b.酸性KMnO4溶液
c.NaOH溶液 d.紫色的石蕊溶液
(2) 试管a中加入几块碎瓷片的目的是______________;
(3) 为了研究乙醇与乙酸反应的机理,若将乙醇中的氧原子用18O标记,写出标记后试管a中发生反应的化学方程式:_________________________________________ ;其反应类型是______________;
(4) 反应开始前,试管b中盛放的溶液是_____________ ;
(5) 反应结束后,常用____________操作把试管b中合成的酯分离出来。
【答案】bd 防止暴沸 CH3COOH+C2H518OH ![]() CH3CO18OC2H5+H2O 取代反应 (或酯化反应) 饱和Na2CO3溶液 分液
CH3CO18OC2H5+H2O 取代反应 (或酯化反应) 饱和Na2CO3溶液 分液
【解析】
(1)乙醇的官能团为-OH,乙酸的官能团为-COOH;
(2)加入几块碎瓷片,可防止液体加热时剧烈沸腾;
(3)乙醇、乙酸发生酯化反应生成乙酸乙酯和水,酯化反应为取代反应;
(4)b中为碳酸钠,可除去乙酸、吸收乙醇、降低乙酸乙酯的溶解度;
(5)试管b中乙酸乙酯与饱和碳酸钠溶液分层;
(1)乙醇分子中官能团的名称是羟基,乙酸中的官能团的结构简式为COOH,羟基能使酸性高锰酸钾褪色,羧基不能使酸性高锰酸钾溶液褪色,羟基不能使石蕊变色,而羧基可以使石蕊变色,
故答案为:bd;
(2)试管a中加入几块碎瓷片的目的是防止暴沸,
故答案为:防止暴沸;
(3)试管a中发生反应的化学方程式为CH3COOH+C2H518OH ![]() CH3CO18OC2H5+H2O,反应类型为酯化(取代)反应,
CH3CO18OC2H5+H2O,反应类型为酯化(取代)反应,
故答案为:CH3COOH+C2H518OH ![]() CH3CO18OC2H5+H2O;酯化(取代)反应;
CH3CO18OC2H5+H2O;酯化(取代)反应;
(4)饱和碳酸钠溶液的作用是溶解乙醇、吸收乙酸、降低乙酸乙酯的溶解度,则反应开始前,试管b中盛放的溶液是饱和碳酸钠溶液,
故答案为:饱和碳酸钠溶液;
(5)试管b中乙酸乙酯与饱和碳酸钠溶液分层,可用分液的方法把制得的乙酸乙酯分离出来,故答案为:分液;


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法正确的是( )
A.含有相同铜原子数的Cu2S和CuO的质量相等B.2g氢气所含质子数目为NA
C.lmol氨气含有的原子数目为2NAD.22.4LCH4所含电子数目为l0NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用于驱动检验管道焊缝设备爬行器的甲醇-燃料电池的工作原理示意如图,下列有关该电池说法正确的是
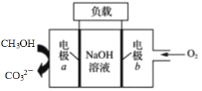
A.该电池工作时,每消耗22.4 L CH3OH转移6 mol电子
B.电子由电极a经负载流向电极b,再经过氢氧化钠溶液返回电极a,形成闭合回路
C.电池工作时,OH-向电极a移动,溶液的pH减小
D.电极b上发生的电极反应为O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g) ![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充入N2使体系压强增大
④保持压强不变,充入N2使容器体积增大
A. ①②B. ①③C. ②③D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组开展模拟工业合成氨的制备实验,在2 L密闭容器内,t℃时发生反应:N2 (g)+3 H2 (g) ![]() 2 NH3 (g),在体系中,n(N2)随时间的变化如下表:
2 NH3 (g),在体系中,n(N2)随时间的变化如下表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1) 上述反应在第5min时,N2的转化率为___________________ ;
(2) 用H2表示从0~2 min内该反应的平均速率v(H2)=______________________;
(3) t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为________________________(用字母填空,下同);
a.v(NH3)=0.05 mol L-1-min-1 b.v(H2)=0.03 mol L-1-min-1
c.v(N2)=0.02mol L-1-min-1 d.v(H2)=0.001 mol L-1- s -1
(4) 下列表述能作为上述实验中可逆反应N2 (g)+3 H2 (g) ![]() 2 NH3 (g) 达到化学平衡状态的标志是_________________________ ;
2 NH3 (g) 达到化学平衡状态的标志是_________________________ ;
a. 反应速率v(N2):v(H2):v(NH3)=1:3:2
b. 各组分的物质的量浓度不再改变
c. 混合气体的平均相对分子质量不再改变
d. 混合气体的密度不变
e. 单位时间内生成n mol N2的同时,生成3n mol H2。
f. v(N2)消耗=2 v(NH3)消耗
g. 单位时间内3mol H﹣H键断裂的同时2mol N﹣H键也断裂
(5) 下列措施不能使上述化学反应速率加快的是_____________。
a.及时分离出NH3气体 b.适当升高温度
c.增大N2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)![]() cC(g)。反应过程中,物质A的体积分数和C的体积分数随温度(T)的变化曲线如图所示,下列说法正确的是( )
cC(g)。反应过程中,物质A的体积分数和C的体积分数随温度(T)的变化曲线如图所示,下列说法正确的是( )
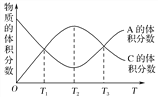
A. 该反应在T1、T3温度时达到化学平衡
B. 该反应在T2温度时达到化学平衡
C. 该反应的逆反应是放热反应
D. 升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据原电池原理,回答下列问题:

(1)图1是依据氧化还原反应:Cu(s)+2Fe3+(aq)=Cu2+(aq)+2Fe2+(aq)设计的原电池装置。
①电极X的材料是________(填化学名称);电极Y的材料是__________(填化学名称)。
②Y电极发生的电极反应式为:______________。
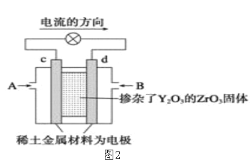
(2)图2是使用固体电解质的燃料电池,装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导正极生成的O2-离子(O2+4e―→2O2-)。
①c电极为______________极。(填“正”或“负”)
②d电极上的电极反应式为___________________________。
③如果消耗甲烷160g,假设化学能完全转化为电能,则转移电子的数目为______________(用NA表示),需要消耗标准状况下氧气的体积为_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C分别是元素甲、乙、丙的单质,它们都是常见的金属或非金属,D、E、F是常见的三种氧化物,且有如图所示转化关系,则下列说法不正确的是( )

A.D、E中一定都含有甲元素
B.单质B肯定是氧化剂
C.A、B、C中一定有一种是氧元素的单质
D.若A是非金属,则B一定为金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌还原四氯化硅是一种有着良好应用前景的制备硅的方法,该制备过程示意图如下:
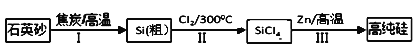
(1)1mol焦炭在过程Ⅰ中失去____mol电子。
(2)过程Ⅱ中Cl2用电解饱和食盐水制备,制备Cl2的离子方程式为________。
(3)步骤(2)中的电解过程中,若用甲醇燃料电池作电源,用KOH作电解质,负极反应为_________。
(4)整过生产过程必须严格控制无水,回答下列问题:
①SiCl4遇水剧烈水解生成SiO2和一种酸,化学反应方程式为_________。
②干燥Cl2时从有利于充分干燥和操作安全的角度考虑,需将约90℃的潮湿氯气先冷却至12℃,然后再通入浓H2SO4中。冷却的作用是_________。
(5)Zn还原SiCl4的可逆反应如下:
SiCl4(g)+2Zn(s)![]() Si(S)+2ZnCl2(g)△H<0下列说法正确的是(___)
Si(S)+2ZnCl2(g)△H<0下列说法正确的是(___)
A.还原过程需在无氧的气氛中进行 |
B.投入1molZn可生成14g还原产物 |
C.增加SiCl4(g)的量,该反应平衡常数不变 |
D.若SiCl4(g)过量可增大△H的值 |
(6)有一种由硅制作的材料中常加入Ag2SO4 ,已知某温度下Ag2SO4(M=312g/mol)的溶解度为0.624g/100g H2O,该温度下Ag2SO4的Ksp=_______(两位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com