
【题目】下图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法确的是( )

A. 31d和33d属于同种核素
B. 气态氢化物的稳定性:a>d>e
C. 工业上常用电解法制备单质b和c
D. a和b形成的化合物不可能含共价键
科目:高中化学 来源: 题型:
【题目】(15分)
重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
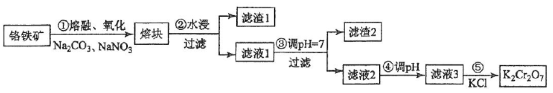
回答下列问题:
(1)步骤①的主要反应为:
FeO·Cr2O3+Na2CO3+NaNO3![]() Na2CrO4+ Fe2O3+CO2+ NaNO2
Na2CrO4+ Fe2O3+CO2+ NaNO2
上述反应配平后FeO·Cr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是________________。
(2)滤渣1中含量最多的金属元素是____________,滤渣2的主要成分是_______________及含硅杂质。
(3)步骤④调滤液2的pH使之变____________________(填“大”或“小”),原因是_________(用离子方程式表示)。
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到___________________(填标号)得到的K2Cr2O7固体产品最多。

a.80℃ b.60℃ c.40℃ d.10℃
步骤⑤的反应类型是___________________。
(5)某工厂用m1 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品 m2 kg,产率为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
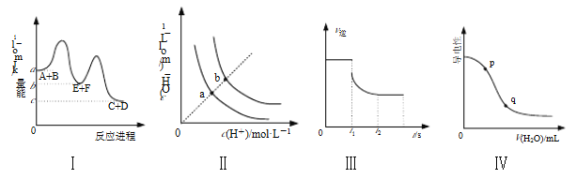
A. 图Ⅰ表示反应A+B=C+D的ΔH=(a-c) kJ·mol-1
B. 图Ⅱ表示不同温度下水溶液中H+和OH-的浓度变化曲线,图中a点对应温度高于b点
C. 图Ⅲ表示N2+3H2![]() 2NH3的v逆随时间变化曲线,由图知t1时刻可能减小了容器内的压强
2NH3的v逆随时间变化曲线,由图知t1时刻可能减小了容器内的压强
D. 图Ⅳ表示向醋酸稀溶液中加水时溶液的导电性变化,图中p点pH大于q点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由C、H、O三种元素组成的某有机物A,在一定条件下,可以转化为有机物B、C和D、E;C又可以转化为B、A。它们的转化关系如下:

已知D的蒸气密度是氢气的22倍,并可以发生银镜反应。
(1)写出下列物质的结构简式:C____, D____;
(2)C→B的反应类型为____;
(3)写出下列转化的化学方程式:
C→A________________________,
A→D________________________,
A+E→F_____________________;
(4)请写出与F具有相同官能团的所有同分异构体的结构简式(不含F):
_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)﹣空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O=4M(OH)n,已知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )

A. 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面
B. 比较Mg,Al,Zn三种金属﹣空气电池,Al﹣空气电池的理论比能量最高
C. M﹣空气电池放电过程的正极反应式:4M++nO2+2nH2O+4ne﹣=4M(OH)n
D. 在Mg﹣空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。 据此下列说法正确的)

A. 该试剂的物质的量浓度为 9.2 mol·L —1
B. 该硫酸 50 mL 与足量的铜反应可得到标准状况下 SO2 10.3 L
C. 配制 200 mL 4.6 mol·L —1 的稀硫酸需取该硫酸 50 mL
D. 该硫酸与等体积的水混合所得溶液的质量分数小于 49%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com