
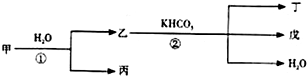
 甲、乙、丙、丁、戊几种中学常见的物质在常温有如图转化关系,在转化过程中,乙与KHCO3按等物质的量混合,并且恰好完全反应.
甲、乙、丙、丁、戊几种中学常见的物质在常温有如图转化关系,在转化过程中,乙与KHCO3按等物质的量混合,并且恰好完全反应.

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32- | ||
| B、无色溶液中:Mg2+、MnO4-、SO42-、K+ | ||
C、
| ||
| D、c(ClO-)=1.0mol?L-1的溶液:Na+、SO32-、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应在前10min内的平均速率为ν(t-BuNO)=0.0375mol?L-1?min-1 |
| B、保持其他条件不变,若此时再向正庚烷反应体系中加入正庚烷,平衡向生成(t-BuNO)2的方向移动 |
C、保持其他条件不变,升高温度,(t-BuNO)2的平衡转化率大于75%,则其能量关系可用图表示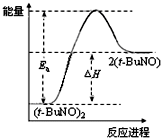 |
| D、保持其他条件不变,若该反应在CCl4中进行,其平衡常数为1.9,则(t-BuNO)2的平衡转化率大于75% |
查看答案和解析>>
科目:高中化学 来源: 题型:
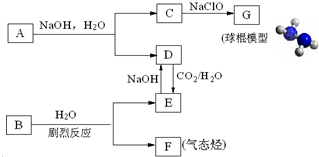
查看答案和解析>>
科目:高中化学 来源: 题型:
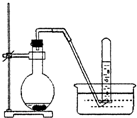 右图是铜与稀硝酸反应的实验装置图,请回答下列问题:
右图是铜与稀硝酸反应的实验装置图,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 条件的变化 | 通氨气 | 加水 | 加NH4Cl(s) | |
| ① | 电离平衡移动的方向 | |||
| ② | c(OH-)的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜片作阴、阳极,电解CuCl2 |
| B、铁片作正极,Cu片作负极,CuCl2作电解质溶液的原电池 |
| C、用铜片作阴、阳极,电解NaOH溶液 |
| D、铜锌合金在潮湿空气中发生电化学腐蚀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com