
| A. | 将乙醛加入新制Cu(OH)2悬浊液中并加热至沸腾,出现红色沉淀 | |
| B. | 将乙醇滴入酸性K2Cr2O7溶液中,溶液由橙色变为绿色 | |
| C. | 将SO2通入滴有酚酞的NaOH溶液中,溶液红色褪去 | |
| D. | 新制氯水敞口处久置,颜色褪去 |
分析 与氧化还原反应无关,说明该反应中没有电子转移,其特征是没有元素化合价升降,据此分析解答.
解答 解:A.CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O,该反应中C元素化合价由-1价变为0价、Cu元素化合价由+2价变为+1价,所以有电子转移,属于氧化还原反应,故A不选;
B.2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O,Cr2O72-转化为Cr3+,C元素化合价由-2价变为0价,有电子转移,所以属于氧化还原反应,故B不选;
C.2NaOH+SO2=Na2SO3+H2O,该反应中各元素化合价不变,没有电子转移,所以不属于氧化还原反应,故C选;
D.氯气与水反应生成次氯酸和盐酸,次氯酸不稳定,见光分解,平衡正向移动,颜色褪去,故D不选;
故选C.
点评 本题考查了氧化还原反应的判断,根据元素化合价是否变化判断即可,注意有机物中元素化合价的判断,取平均化合价,为易错点.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 主要实验步骤及实验现象 |
| ① | 在含Y的溶液中,加入稀硫酸放置,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色 |
| ② | 在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀 |
| ③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
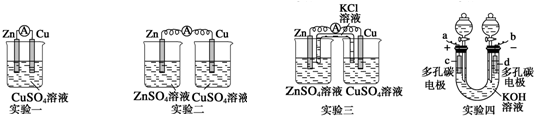
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| W | X | ||
| Y | Z |
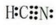 ;
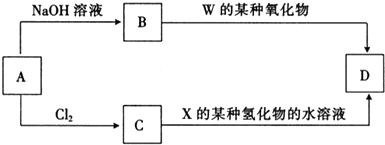
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| A | CCl4 | Br2 | 用NaOH溶液洗涤、分液 |
| B | FeCl3 | CaCO3 | 溶解、过滤、蒸发结晶 |
| C | Al2(SO4)3溶液 | MgSO4 | 加入过量烧碱后过滤,再用硫酸酸化滤液 |
| D | CO2 | SO2 | 通过盛有品红溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com