
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:推断题
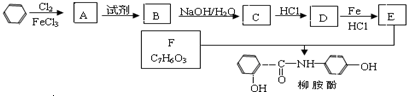
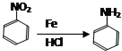
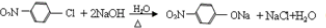 .
.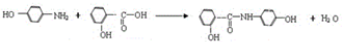 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 金属钠投入水中,浮在水面熔成小球,并在水面快速移动,得到的溶液显碱性;2 Na+2 H2O═2 NaOH+H2↑ | |
| B. | 氢气在氯气中安静的燃烧,发出淡蓝色火焰,瓶口出现白雾;H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl | |
| C. | FeSO4溶液中加入NaOH溶液时,生成的白色絮状沉淀迅速变为灰绿色,最后变成红褐色; 2Fe(OH)2+O2+H2O═2 Fe(OH)3 | |
| D. | 向Na2SiO3溶液中逐滴加入稀盐酸,边加边振荡,有透明的硅酸凝胶产生;Na2SiO3+2HCl═H2SiO3(胶体)+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应达到化学平衡状态的正逆反应速率相等,是指同一物质的消耗速率和生成速率相等,若用不同物质表示时,反应速率不一定相等 | |
| B. | 标准状况下,1 L辛烷完全燃烧生成CO2 8 L | |
| C. | 2.4 g Mg无论与O2还是与N2完全反应,转移电子数都是0.2NA | |
| D. | 1 L 1 mol•L-1 CH3COOH溶液中,所含CH3COO-、CH3COOH的总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.4mol/(L•s) | B. | v(B)=0.5mol/(L•s) | C. | v(C)=0.6mol/(L•s) | D. | v(D)=0.7mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,向醋酸溶液中加入少量的水,溶液中c(H+)将增大 | |
| B. | 常温下,2NO(g)+2CO(g)?N2(g)+2CO2(g)能自发进行,则该反应的△H<0 | |
| C. | 硫酸铜饱和溶液降低温度时有晶体析出,可用熵判据来解释 | |
| D. | 用CH3COOH溶液做导电实验,灯泡很暗,一定能证明CH3COOH是弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、K+、Ca2+、HCO3- | B. | OH-、Cl-、Na+、NH${\;}_{4}^{+}$ | ||
| C. | Cu2+、Na+、SO42-、Cl- | D. | Mg2+、Na+、Cl-、CH3COO- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com