
一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:N2+3H2O 2NH3+O2
2NH3+O2
进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):
T/℃ | 30 | 40 | 50 |
生成NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
请回答下列问题:
(1)50℃时从开始到3 h内以O2物质的量变化表示的平均反应速率为________ mol·h-1。
(2)该反应过程与能量关系可用如图表示,则反应的热化学方程式是____________。

(3)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢。请提出可提高其反应速率且增大NH3生成量的建议:_______________________________________。
(4)工业合成氨的热化学方程式为N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1。在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。求:
2NH3(g) ΔH=-92.4 kJ·mol-1。在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。求:
①该条件下的平衡常数为________;
②若向该容器中加入a mol N2、b mol H2、c mol NH3,且a、b、c均大于0,在相同条件下达到平衡时,混合物中各组分的物质的量与上述平衡相同。反应放出的热量________(填“>”“<”或“=”)92.4 kJ。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014年高中化学鲁科版选修四第3章 物质在水溶液中的行为练习卷(解析版) 题型:选择题
有体积相同、pH相等的烧碱溶液和氨水,下列叙述中正确的是( )
A.两溶液物质的量浓度相同
B.用同浓度的盐酸中和时,消耗盐酸的体积相同
C.两溶液中OH-浓度相同
D.加入等体积的水稀释后,pH仍相等
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四模块综合检测练习卷(解析版) 题型:选择题
在一个绝热的体积一定的密闭容器中发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,下列各项中不能说明该反应已经达到化学平衡状态的是( )
2NH3(g) ΔH<0,下列各项中不能说明该反应已经达到化学平衡状态的是( )
A.体系的压强不再改变
B.体系的温度不再改变
C.断裂1 mol N≡N键的同时,也断裂6 mol N—H键
D.反应消耗的N2、H2与产生的NH3的速率v(N2)∶v(H2)∶v(NH3)=1∶3∶2
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题3 溶液中的离子反应练习卷(解析版) 题型:选择题
下列叙述正确的是( )
A.中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠多于醋酸
B.将氢氧化钠溶液和氨水各稀释一倍,两者的c(OH-)均减少到原来的一半
C.常温下,某溶液中由水电离出的c(OH-)=1×10-10 mol/L,该溶液可能是盐酸
D.如果盐酸的物质的量浓度是醋酸的两倍,则盐酸的c(H+)也是醋酸的两倍
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题3 溶液中的离子反应练习卷(解析版) 题型:选择题
常温下pH最小的是下列各项中的( )
A.pH=0的溶液 B.0.04 mol·L-1H2SO4
C.0.5 mol·L-1HCl D.0.05 mol·L-1CH3COOH
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题2 反应速率与化学平衡练习卷(解析版) 题型:填空题
可逆反应:aA(g)+bB(g) cC(g)+dD(g);ΔH=Q,试根据图回答:
cC(g)+dD(g);ΔH=Q,试根据图回答:

(1)压强p1比p2________(填“大”、“小”)。
(2)(a+b)比(c+d)________(填“大”、“小”)。
(3)温度t1℃比t2℃________(填“高”、“低”)。
(4)Q值是________(填“正”、“负”)。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题2 反应速率与化学平衡练习卷(解析版) 题型:选择题
在容积不变的密闭容器中存在如下反应:2A(g)+B(g) 3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
3C(g);ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

A.图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响
B.图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高
D.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题1 化学反应与能量变化练习卷(解析版) 题型:选择题
2010年10月1日,我国在西昌卫星发射中心成功发射“嫦娥二号”。嫦娥二号火箭推进器以联氨(N2H4)为燃料、过氧化氢为助燃剂。已知下列各物质反应的热化学方程式为
N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH1=-533.23 kJ·mol-1
H2O(g)=H2O(l);ΔH2=-44 kJ·mol-1
2H2O2(l)=2H2O(l)+O2(g);ΔH3=-196.4 kJ·mol-1
则联氨与过氧化氢反应的热化学方程式可表示为( )
A.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);ΔH=+817.63 kJ·mol-1
B.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);ΔH=-641.63 kJ·mol-1
C.N2H4(g)+2H2O2(l)=N2(g)+4H2O(l);ΔH=-641.63 kJ·mol-1
D.N2H4(g)+2H2O2(l)=N2(g)+4H2O(g);ΔH=-817.63 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014年高中化学人教版选修四第二章 化学反应速率与化学平衡练习卷(解析版) 题型:填空题
现有下列可逆反应:A(g)+B(g)  xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
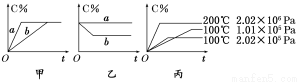
请根据图像回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况(填字母,下同);
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性(与反应体系中任一物质均不反应)气体后的情况,则 曲线表示恒温恒容的情况;
(3)根据丙图可以判断该可逆反应的正反应是 热反应(填“吸”或“放”);
(4)化学计量数x的值 (填取值范围);判断的依据是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com