
| A. | Na2S溶液:c(Na+)>c(S2-)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2CO3溶液:c(Na+)+c(H+)=c(CO${\;}_{3}^{2-}$)+c(HCO${\;}_{3}^{-}$)+c(OH-) | |
| C. | Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O${\;}_{4}^{-}$)+2c(H2C2O4) | |
| D. | CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
分析 A.氢氧根离子来自水的电离和硫离子的水解,则c(OH-)>c(HS-);
B.根据碳酸氢钠溶液中的电荷守恒判断;
C.根据Na2C2O4溶液中的质子守恒判断;
D.根据混合液中的物料守恒分析.
解答 解:A.硫化钠溶液中,硫离子部分水解,溶液呈碱性,由于氢氧根离子来自水的电离和硫离子的水解,则c(OH-)>c(HS-),正确的离子浓度大小为:c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H2S),故A错误;
B.Na2CO3溶液中满足电荷守恒:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-),故B错误;
C.根据Na2C2O4溶液中的质子守恒可得:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4),故C正确;
D.CH3COONa和CaCl2混合溶液中,根据物料守恒可得:即:c(Na+)=c(CH3COO-)+c(CH3COOH)、2c(Ca2+)=c(Cl-),则:c(Na+)+2c(Ca2+)=c(CH3COO-)+c(CH3COOH)+c(Cl-),故D错误;
故选C.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理、核电荷数、物料守恒及质子守恒的含义为解答关键,A为易错点,注意氢氧根离子来自水的电离和硫离子的水解,试题培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 冰融化一一共价键 | B. | 二氧化硅熔融--范德华力 | ||
| C. | 氢氧化钠溶于水--离子键、共价键 | D. | 硫酸氢钠溶于水--离子键、共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体系的压强不再发生变化 | |
| B. | v(CO2)=v(H2O) | |
| C. | 生成n mol CH3OH的同时生成n mol H2O | |
| D. | 3 mol H-H键断裂的同时断裂2 mol H-O键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
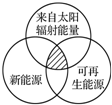
| A. | 沼气、煤炭、石油 | B. | 海洋能、地热能、核能 | ||
| C. | 天然气、水能、生物能 | D. | 风能、太阳能、潮汐能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 邻二甲苯属于芳香烃,它的官能团是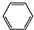 | |
| B. | 分子结构 是维生素A的键线式 是维生素A的键线式 | |
| C. | 氯溴碘代甲烷的同分异构体数目有两个,就像人的左右手似的 | |
| D. | 乙醇与二甲醚互为同分异构体,这种同分异构现象叫官能团异构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 名称 | 化学式 | △H(kJ•mol-1) |
| ① | 石墨 | C(s) | -393.5 |
| ② | 金刚石 | C(s) | -395.4 |
| ③ | 氢气 | H2(g) | -285.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都正确 | B. | ③④ | C. | ①② | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
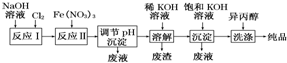
| A. | 反应Ⅰ主要为2NaOH+Cl2═NaCl+NaClO+H2O 反应Ⅱ的离子方程式为3ClO-+10OH-+2Fe3+═2FeO42-+3Cl-+5H2O | |
| B. | 加入饱和KOH溶液的目的是增大K+浓度,促进K2FeO4晶体析出 | |
| C. | 调节pH析出的沉淀为高铁酸钠,用异丙醇洗涤的主要目的是有利于产品干燥 | |
| D. | 高铁酸钾是一种理想的水处理剂,其处理水的原理为高铁酸钾有强氧化性,能杀菌消毒,产生的Fe(OH)3有吸附性,有絮凝作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com