
分析 (1)B遇浓盐酸产生“白烟”,则B为氨气,A是常用的中性干燥剂,则A为氯化钙,所以实验室制氨气的反应符合X+Y→A+B(g)+C(1)转化关系;
(2)B呈黄绿色,则B为氯气,X为氧化物,则实验室制氯气的反应符合X+Y→A+B(g)+C(1)转化关系;
(3)B为氧化物且能使品红溶液腿色,则B为二氧化硫,X为红色固体单质,则X为铜,Y为浓硫酸,铜与浓硫酸反应生成二氧化硫、硫酸铜和水的反应符合X+Y→A+B(g)+C(1)转化关系;
(4)B遇空气变红棕色,则B为NO,X为Cu2O,Y为稀硝酸,Cu2O与稀硝酸反应生成NO、硝酸铜和水的反应符合X+Y→A+B(g)+C(1)转化关系;
解答 解:(1)B遇浓盐酸产生“白烟”,则B为氨气,A是常用的中性干燥剂,则A为氯化钙,所以实验室用氯化铵与氢氧化钙加热制氨气,反应的方程式为NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑,符合X+Y→A+B(g)+C(1)转化关系,则盐X的化学式为NH4Cl,故答案为:NH4Cl;CaCl2
;
(2)B呈黄绿色,则B为氯气,X为氧化物,所以实验室用二氧化锰与浓盐酸加热制氯气,反应的方程式为4HCl+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑,符合X+Y→A+B(g)+C(1)转化关系,则Y的化学式为HCl;A为MnCl2,因为MnCl2溶液易发生水解生成挥发性的酸,所以获得无水A的操作是在HCl的气流中蒸发;故答案为:HCl;在HCl的气流中蒸发;
(3)B为氧化物且能使品红溶液腿色,则B为二氧化硫,X为红色固体单质,则X为铜,Y为浓硫酸,铜与浓硫酸反应生成二氧化硫、硫酸铜和水的反应符合X+Y→A+B(g)+C(1)转化关系,所以A的化学式为CuSO4;故答案为:CuSO4;
(4)B遇空气变红棕色,则B为NO,X为Cu2O,Y为稀硝酸,Cu2O与稀硝酸反应生成NO、硝酸铜和水的反应符合X+Y→A+B(g)+C(1)转化关系,离子方程式为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O;故答案为:3Cu2O+14H++2NO3-=6Cu2++2NO↑+7H2O.
点评 以物质转化关系的形式考查元素单质及其化合物的性质,难度中等,在熟练掌握元素化合物知识的基础上着重考查学生的发散思维、分析判断、逻辑思维以及对无机物知识的综合应用等能力.


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:解答题
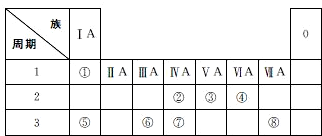
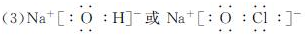 .
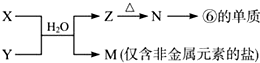
.
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
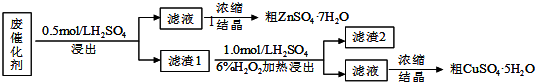
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 生成气体的质量可能是11克或33克 | |
| B. | 滤渣中的红色物质可能是32克或96克 | |
| C. | 参与反应的氧化铜质量可能是40克或120克 | |
| D. | 稀硫酸的溶质质量可能是38.4克或115.2克 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用湿润的pH试纸测稀碱液的,测定值偏小 | |
| B. | 用量筒量取10mLNaOH 溶液时,俯视刻度.量出的体积大于10mL | |
| C. | 使用天平称量时不小心将药品与砝码的位置放反了,称最结果可能是准确的 | |
| D. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与稀盐酸反应放出气体的快慢:Na2CO3>NaHCO3 | |
| B. | 配制成同物质的量浓度的溶液时,溶液的pH:Na2CO3>NaHCO3 | |
| C. | 106gNa2CO3和84gNaHCO3分别与过量的盐酸反应,放出CO2的质量:Na2CO3>NaHCO3 | |
| D. | 在Na2CO3和NaHCO3的稀溶液中,加CaCl2溶液都有白色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com