
����Ŀ��ʵ������ȡ���ռ�������װ������ͼ��ʾ����ش���������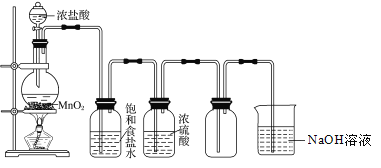
��1�����巢��װ���н��еķ�Ӧ��ѧ����ʽ��______
��2����0.5mol MnO2���뷴Ӧʱ����������HCl������Ϊ ______ �����ɵ�Cl2�ڱ�״���µ����ԼΪ ______ ��
��3����װ���У��ٱ���ʳ��ˮ�������� ______ ����Ũ����������� ______ ��
��4����ѧʵ���м����Ƿ���Cl2��������ʪ��ĵ���-KI��ֽ�������Cl2�������ɹ۲쵽��������______ ��
��5��д��β������װ���н��еķ�Ӧ�����ӷ���ʽ______ ��
���𰸡� ![]() 36.5g 11.2L ��ȥCl2�е�HCl �������� ��ֽ���� Cl2+2OH-=Cl-+ClO- +H2O
36.5g 11.2L ��ȥCl2�е�HCl �������� ��ֽ���� Cl2+2OH-=Cl-+ClO- +H2O
����������1�����巢��װ���н��еķ�Ӧ�Ƕ�����������Ũ���ᣬ��Ӧ�Ļ�ѧ����ʽ��MnO2+4HCl(Ũ)![]() MnCl2+Cl2+2H2O����2����0.5molMnO2���뷴Ӧʱ����������HCl�����ʵ�����1mol������Ϊ36.5g������0.5molCl2���ڱ�״���µ����ԼΪ11.2L����3�����ɵ������к��лӷ������Ȼ��⣬��ˢ��б���ʳ��ˮ�������dz�ȥCl2�е�HCl����Ũ����������Ǹ�����������4����������ǿ�����ԣ��ܰѵ⻯���������ʵ⣬������������ɫ��������������������ɹ۲쵽����������ֽ��������5�������ж�����Ҫβ����������Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO- +H2O��
MnCl2+Cl2+2H2O����2����0.5molMnO2���뷴Ӧʱ����������HCl�����ʵ�����1mol������Ϊ36.5g������0.5molCl2���ڱ�״���µ����ԼΪ11.2L����3�����ɵ������к��лӷ������Ȼ��⣬��ˢ��б���ʳ��ˮ�������dz�ȥCl2�е�HCl����Ũ����������Ǹ�����������4����������ǿ�����ԣ��ܰѵ⻯���������ʵ⣬������������ɫ��������������������ɹ۲쵽����������ֽ��������5�������ж�����Ҫβ����������Ӧ�����ӷ���ʽΪCl2+2OH-=Cl-+ClO- +H2O��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��COCl2(g)![]() CO(g)��Cl2(g) ��H>0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������� �ں���ͨ��������� ������COŨ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2ת���ʵ���
CO(g)��Cl2(g) ��H>0������Ӧ�ﵽƽ��ʱ�����д�ʩ�������� �ں���ͨ��������� ������COŨ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2ת���ʵ���
A���٢ڢ� B���ڢۢ� C���ۢݢ� D���٢ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��Ϊ�л����������֮��Ĺ�ϵ������ʾ(��ʾ��RCH===CHR����KMnO4������Һ�з�Ӧ����RCOOH��R��COOH������R��R��Ϊ���)

�ش��������⣺
(1)ֱ��������A����Է�������С��90��A������̼����Ԫ�ص�����������Ϊ0.814������Ϊ��Ԫ�أ���A�ķ���ʽΪ____________��
(2)��֪B��NaHCO3��Һ��ȫ��Ӧ�������ʵ���֮��Ϊ12������Ũ����Ĵ��£�B��������C2H5OH������Ӧ�Ļ�ѧ����ʽ��___________________����Ӧ����Ϊ________��
(3)A��������������÷ų���������ʹ���CCl4��Һ��ɫ����A�Ľṹ��ʽ��___________________��
(4)D��ͬ���칹���У�����NaHCO3��Һ��Ӧ�ų�CO2����________�֣�����Ӧ�Ľṹ��ʽΪ__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���д�������� ��
A��������ѧϰ���о���ѧ���ʼ���仯��һ�ֳ��÷���
B����ЩҺ̬����Ҳ�����ģ������ۺ�������Һ������
C��2L1 mol/L Na2CO3��Һ�� c ��Na+��Ϊ4 mol/L
D����1LNaCl��Һ��ȡ��100 ml����Ũ����ԭlL��Һ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȥ���������е�����(�����ڵ�����)����ʹ�õ��Լ�����Ҫ��������ȷ����
ѡ�� | ���� | ʹ�õ��Լ� | ��Ҫ���� |
A | �Ҵ���ˮ�� | ������ | ���� |
B | �������������ᣩ | ����̼������Һ | ��Һ |
C | �������ӣ� | Ũ��ˮ | ���� |
D | ���飨��ϩ�� | ���Ը��������Һ | ϴ�� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л����ϵͳ��������ȷ���� ( )
A��3������4���һ����� B��3,3,4����������
C��3,4,4���������� D��3,5����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ļ�����ϳɡ�Ӧ�ü����Ĺ̶�һֱ�ǿ�ѧ�о����ȵ㡣
��1����CO2��NH3Ϊԭ�Ϻϳɻ������ص���Ҫ��Ӧ���£�
��2NH3��g����CO2��g����NH2CO2NH4��s������H����159.47 kJ��mol��1
��NH2CO2NH4��s����CO��NH2��2��s����H2O��g������H��a kJ��mol��1
��2NH3��g����CO2��g����CO��NH2��2��s����H2O��g������H����86.98 kJ��mol��1
��aΪ ��
��2����Ӧ2NH3��g����CO2��g��![]() CO��NH2��2��s����H2O��g�� �ںϳ����н��С���ͼ1��������������������Ϊ�ϳ����а���ͬ��̼�� [n��NH3��/n��CO2��]��ˮ̼��[n��H2O��/n��CO2��]Ͷ��ʱ������̼ת���ʵ������
CO��NH2��2��s����H2O��g�� �ںϳ����н��С���ͼ1��������������������Ϊ�ϳ����а���ͬ��̼�� [n��NH3��/n��CO2��]��ˮ̼��[n��H2O��/n��CO2��]Ͷ��ʱ������̼ת���ʵ������

ͼ1 ͼ2 ͼ3
����������������ˮ̼�ȵ���ֵ�ֱ�Ϊ��
A. 0.6��0.7 B. 1��1.1 C. 1.5��1.61
������Ӧѡ��ˮ̼�ȵ���ֵΪ ��ѡ����ţ���
�������а�̼���˿�����4.0���ң�������4.5��ԭ������� ��
��3�����ؿ�����ʪ�������ѵ����գ��䷴Ӧԭ��Ϊ��
NO��NO2��H2O��2HNO2��2HNO2��CO��NH2��2��2N2����CO2����3H2O��
����������NO��NO2��������Ӧ��ϵ����ʱ�ѵ�Ч����ѡ���������V��NO����V��NO2����5��1ʱ����ͨ��һ�����Ŀ�����ͬ��ͬѹ�£�V����������V��NO���� �����������������������ԼΪ20%����
��ͼ2�����غ������ѵ�Ч�ʵ�Ӱ�죬�Ӿ��������Ͽ��ǣ�һ��ѡ������Ũ��ԼΪ %��
��4��ͼ3��ʾʹ�����͵缫���ϣ���N2��H2Ϊ�缫��Ӧ���HCl��NH4ClΪ�������Һ����������ṩ������ͬʱ����ʵ�ֵ��̶�������ȼ�ϵ�ء���д���õ�ص�������Ӧʽ �������пɷ����������A�Ļ�ѧʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������п����������Ϳ�ϡ��մɡ�ҽҩ�����ӵ���ҵ���Ź㷺��Ӧ�ã���ͼ���Ժ�пͭ�̳�������ͭ�ĸ���Ʒ����Ҫ�ɷ���ZnO��CuO��FeO���Ʊ���������п�Ĺ������̣�

��֪����пͭ�̳�����Ԥ���������Ҫ�ɷ���ZnO��������������CuO��Fe2O3��
��1�� �ܽ���д�����ȫ���ܽ����п�۵������У�
�� ��Fe3����ԭΪFe2����
�� ____________��
�� ������Һ��pH��
��2�� �����ܽ����Fe3����ȫ������ԭΪFe2����ʵ�鷽����________________��
��3�� ��Ӧ���е��¶ȿ�����90��95 ��������BΪ���������Ӧ������������Ӧ�����ӷ���ʽΪ________________��
��4�� �������еõ��ij�����ѧʽ���Ա�ʾΪaZnCO3��bZn��OH��2��cH2O��a��b��c��Ϊ��������ijУ��ѧ��ȤС���ͬѧΪ��ȷ������ɣ���������ʵ�飺��ȡ3.59 g�������б��գ������չ����в�������������ͨ��������Ũ����ͼ�ʯ�ң����Ƿֱ�����0.72 g��0.44 g��ͨ������ȷ���ó�������ɡ���д�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��I2+2S2O32-=S4O62-+2I-��������ʵ��ܶȻ��������±���
���� | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2��10��20 | 2.6��10��29 | 1.7��10��7 | 1.3��10��12 |
��1��ij����CuCl2��Һ�к���������FeCl3��Ϊ�õ�������CuCl2�q2H2O���壬���� ����pH��4��ʹ��Һ�е�Fe3+ת��ΪFe(OH)3��������ʱ��Һ�е�c(Fe3+)�� �����˺�������Һ����������Ũ���ᾧ���ɵõ�CuCl2�q2H2O���塣
��2���ڿ�����ֱ�Ӽ���CuCl2�q2H2O����ò���������ˮCuCl2��ԭ���� ��(�û�ѧ����ʽ��ʾ)����CuCl2�q2H2O����õ�������ˮCuCl2�ĺ��������� ��
��3��ijѧϰС���á���ӵ��������ⶨ����CuCl2�q2H2O���������(��������I�D������Ӧ��������������)�Ĵ��ȣ��������£�ȡ0.36 g��������ˮ���������KI���壬��ַ�Ӧ�����ɰ�ɫ��������0.1000 mol��L-1Na2S2O3����Һ�ζ�������ζ��յ�ʱ������Na2S2O3����Һ20.00 mL��
�ٿ�ѡ�� ���ζ�ָʾ�����ζ��յ�������� ��
��CuCl2��Һ��KI��Ӧ�����ӷ���ʽΪ ��
�۸�������CuCl2�q2H2O�������ٷ���Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com