


分析 根据题中工业流程,重晶石矿(主要成分BaSO4,杂质为Fe2O3、SiO2)与碳在焙烧的条件下得BaS、Fe,SiO2不反应,用盐酸酸溶后,BaS与盐酸反应得硫化氢和氯化钡,铁与盐酸反应生成氢气和氯化亚铁,SiO2不溶,不溶物A应为SiO2,由于流程最后要得到氯化钡晶体,所以沉淀反应中加入的试剂R可以为氧化钡或氢氧化钡等,沉淀物B应为氢氧化铁,经过蒸发浓缩、降温结晶、过滤、洗涤、干燥等操作可得氯化钡晶体,
(1)根据流程分析A的成分,焙烧得到气体为一氧化碳;
(2)根据配制一定物质的量浓度溶液的操作可以确定所需要的仪器;
(3)试剂R的作用是将铁离子沉淀掉,且不引入新的杂质;沉淀反应主要是将铁离子沉淀完全;
(4)将BaCl2•nH2O充分加热失去结晶水,根据加热前后固体物质的质量可以确定n值;根据实验对恒重的要求答题;空气中有水份,对实验有影响;
(5)重晶石矿与碳以及氯化钙共同焙烧,可以直接得到氯化钡,由于硫化钙不溶于水,所以将焙烧得的固体直接溶于水,过滤除去固体杂质,可以得到氯化钡溶液,为了溶解充分可以用热水,滤液经过蒸发浓缩、降温结晶、过滤、洗涤、干燥可得氯化钡晶体;
解答 解:根据题中工业流程,重晶石矿(主要成分BaSO4,杂质为Fe2O3、SiO2)与碳在焙烧的条件下得BaS、Fe,SiO2不反应,用盐酸酸溶后,BaS与盐酸反应得硫化氢和氯化钡,铁与盐酸反应生成氢气和氯化亚铁,SiO2不溶,不溶物A应为SiO2,由于流程最后要得到氯化钡晶体,所以沉淀反应中加入的试剂R可以为氧化钡或氢氧化钡等,沉淀物B应为氢氧化铁,经过蒸发浓缩、降温结晶、过滤、洗涤、干燥等操作可得氯化钡晶体,
(1)根据流程分析A的成分为C和SiO2,焙烧得到气体为一氧化碳,可以用点燃的方法进行处理,故选c,
故答案为:SiO2;c;
(2)根据配制一定物质的量浓度溶液的操作可知所需要的玻璃仪器为玻璃棒、烧杯、500mL容量瓶、胶头滴管,
故答案为:烧杯、500mL容量瓶、胶头滴管;
(3)试剂R的作用是将铁离子沉淀掉,且不引入新的杂质,试剂R可以为氧化钡,证明沉淀已经完全的方法是取上层清液于小试管中,滴入氢氧化钠溶液,若无沉淀产生,说明沉淀完全,
故选b;取上层清液于小试管中,滴入氢氧化钠溶液,若无沉淀产生,说明沉淀完全;
(4)将BaCl2•nH2O充分加热失去结晶水,根据加热前后固体物质的质量可以确定n值,所以实验步骤为①称量样品 ②加热 ③置于干燥器中冷却 ④称量 ⑤恒重操作,恒重操作是指再进行加热、冷却、称量,直到连续两次称量的结果相差不超过0.001g为止,第③步物品之所以放在干燥器中冷却的原因是防止冷却过程中吸收空气中的水分,造成实验误差,
故答案为:加热;干燥器;再进行加热、冷却、称量,直到连续两次称量的结果相差不超过0.001g为止;防止冷却过程中吸收空气中的水分,造成实验误差;
(5)重晶石矿与碳以及氯化钙共同焙烧,可以直接得到氯化钡,由于硫化钙不溶于水,所以将焙烧得的固体直接溶于水,过滤除去固体杂质,可以得到氯化钡溶液,为了溶解充分可以用热水,滤液经过蒸发浓缩、降温结晶、过滤、洗涤、干燥可得氯化钡晶体,
故答案为:热水浸取;蒸发浓缩;冷却结晶;过滤.
点评 本题考查学生在“工艺流程阅读、相关反应化学方程式书写、化学反应条件控制的原理、生产流程的作用”等方面对元素化合物性质及其转化关系的理解和应用程度,考查学生对新信息的处理能力,题目难度中等.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3COOH+CH3CH2OH$→_{加热}^{浓硫酸}$CH3COOCH2CH33+H2O | |
| B. | 2CH3CH2OH+O2 $→_{△}^{催化剂}$ 2CH3CHO+2H2O | |
| C. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| D. | 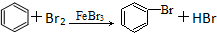 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子符号 | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 2.5 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇(水) 加新制的生石灰,过滤 | |
| B. | 乙烷(乙烯) 通过溴的四氯化碳溶液,洗气 | |
| C. | 溴(苯) 加水,振荡,静置后分液 | |
| D. | 乙酸乙酯(乙酸) 加饱和Na2CO3溶液,振荡,静置后分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com