
 ��g��?3H2��g��+
��g��?3H2��g��+ ��g����H1
��g����H1 ��g��+H2��g����
��g��+H2��g���� ��g����H2=+28.6KJ/mol
��g����H2=+28.6KJ/mol ��g��+2H2��g����
��g��+2H2��g���� ��g����H3=-237KJ•mol-1
��g����H3=-237KJ•mol-1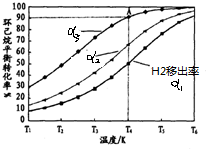
���� ��1�����ݸ�˹���ɣ��� ��g��+H2��g����
��g��+H2��g���� ��g����H2=+28.6KJ/mol����
��g����H2=+28.6KJ/mol���� ��g��+2H2��g����
��g��+2H2��g���� ��g����H3=-237KJ•mol-1����H1=-��-�ڣ��ɴ˷������
��g����H3=-237KJ•mol-1����H1=-��-�ڣ��ɴ˷������
��2����������ʽ��ϻ������ת������ƽ��ʱ����ֵ�����Ȼ����빫ʽ���м��㣻
��3��������Ĥ��Ӧ����Ŀ���Ƿ�������ɵ�������ƽ�������ƶ������������IJ��ʻ�Ӧ���ת���ʣ�
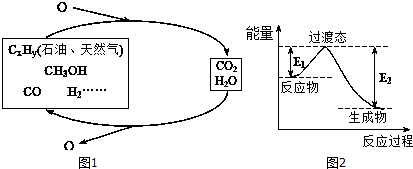
����ͼ��֪ͬ���������Ƴ���Խ�������ת����Խ�ߣ�
��4�����ص������Ϸ���ʧ���ӵ�������Ӧ���ݴ���д�缫��Ӧʽ��
��� �⣺��1�����ݸ�˹���ɣ��� ��g��+H2��g����
��g��+H2��g���� ��g����H2=+28.6KJ/mol����
��g����H2=+28.6KJ/mol���� ��g��+2H2��g����
��g��+2H2��g���� ��g����H3=-237KJ•mol-1����H1=-��-��=237-28.6=+208.4KJ•mol-1���ʴ�Ϊ��+208.4KJ•mol-1��
��g����H3=-237KJ•mol-1����H1=-��-��=237-28.6=+208.4KJ•mol-1���ʴ�Ϊ��+208.4KJ•mol-1��
��2��ij�¶��£�1.00mol���������ݻ�Ϊ1.00L���ܱ������з�Ӧ�з�Ӧ���ﵽƽ��ʱѹǿ��ԭ����3.80����
 ��g��?3H2��g��+
��g��?3H2��g��+ ��g��
��g��
��������1mol 0 0
ת������x 3x x
ƽ������1-x 3x x
��1+3x=3.8����֮�ã�x=0.93������ת����Ϊ��$\frac{0.93}{1}��100%$=93.3%���ʴ�Ϊ��93.3%��
��3��������Ĥ��Ӧ����Ŀ���Ƿ�������ɵ�������ƽ�������ƶ������������IJ��ʻ�Ӧ���ת���ʣ��ʴ�Ϊ����߲��ʻ�ת���ʣ�
����ͼ��֪ͬ���������Ƴ���Խ�������ת����Խ�ߣ�����ƽ�������ƶ�Խ�࣬ת����Խ�ߣ��ʴ�Ϊ��ͬ���£������Ƴ���Խ�ߣ��������ת����Խ�ߣ�ƽ�������ƶ�Խ�࣬ת����Խ�ߣ�
��4���ѻ�����ת��Ϊ�����������ǻ�����ʧ���ӵ�������Ӧ���缫��ӦΪ��C6H14-6e-=6H++C6H6���ʴ�Ϊ��C6H14-6e-=6H++C6H6��
���� �����ۺϿ���ѧ���Ȼ�ѧ���绯ѧ�Լ���ѧƽ����йؼ���֪ʶ�������ۺ�֪ʶ�Ŀ��飬�ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ˮ���Ӽ���ڦм� | B�� | ˮ���Ӽ������� | ||
| C�� | ˮ������V�νṹ | D�� | ˮ�����Ǽ��Է��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬһԪ�ز����ܼȱ��ֽ����ԣ��ֱ��ַǽ����� | |
| B�� | ������������Ԫ�ص���������ϼ۵������������������� | |
| C�� | ������Ԫ��ԭ���γɼ����Ӻ��������Ӷ��ﵽ8�����ȶ��ṹ | |
| D�� | ͬһ�����Ԫ�ص�ԭ�ӣ�������������ͬ����ѧ������ȫ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� | �� | �� | �� | |
| �� | �� | �� |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| C-H | C-O | C=O | H-H | H-O |
| 413.4 | 351 | 745 | 436 | 462.8 |
| ʵ�� | �¶�/�� | ��ʼ�� | �ﵽƽ�� | |||
| CO/mol | H2O/mol | H2/mol | COת���� | ����ʱ��/min | ||
| 1 | 650 | 4 | 2 | 1.6 | 6 | |
| 2 | 900 | 2 | 1 | 1/3 | 3 | |
| 3 | 900 | a | b | c | t | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯӢ�����ռ���Һ��SiO2+2OH-�TSiO32-+H2O | |
| B�� | ����������Һ��ͨ�������Ķ�������SO2+OH-�THSO3- | |
| C�� | ̼�������Һ�м�����������������Һ��Ca2++HCO3-+OH-�TCaCO3��+H2O | |
| D�� | �廯������Һ��ͨ������������2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Ħ��ˮ��Ħ��������1Ħ��ˮ��Ħ������ | |
| B�� | 1mol/L�Ȼ�����Һ��n��Cl-����2mol/L�Ȼ�����Һ��n��Cl-�� | |
| C�� | 20%NaOH��Һ��NaOH�����ʵ���Ũ�Ⱥ�10%NaOH��Һ��NaOH�����ʵ���Ũ�� | |
| D�� | 64�˶�����������ԭ�����ͱ�״����22.4��һ����̼����ԭ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com