
| A、标准状况下,11.2L氯仿(CHCl3)中含有C-Cl键的数目为1.5NA |
| B、0.05mol熔融的KHSO4中含有阳离子的数目为0.05NA |
| C、500℃、30MPa下:N2(g)+3H2(g)?2NH3(g);△H=-38.6kJ?mol-1;将1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3kJ |
| D、常温常压下,17g甲基(-14CH3)所含的中子数为9NA |


科目:高中化学 来源: 题型:
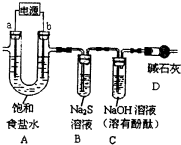 A为用惰性电极电解饱和食盐水的装置.
A为用惰性电极电解饱和食盐水的装置.| 假设 | 验证假设的主要操作 | 预期现象 | 结论 |
|
假设1: |
|||
| 假设2:可能是发生中和反应,导致溶液退色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温下,16g O2和O3的混合气体中含有NA个氧原子 |
| B、2.24L HCl气体中含有0.1NA个HCl分子 |
| C、将0.1mol FeCl3溶于1L水中,所得溶液中含有0.1NA个Fe3+ |
| D、25℃时,1L pH=13的Ba(OH)2溶液中含有0.2 NA个OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 二氧化锰与浓盐酸反应制干燥氯气 |
B、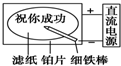 滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用外加保护膜的细铁棒做笔在滤纸上写字显红色字迹 |
C、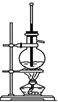 石油的分馏 |
D、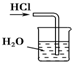 用水吸收氯化氢气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Cu2+、Cl-、SO42- |
| B、Al3+、Na+、Cl-、NO3- |
| C、Ag+、K+、SO42-、Cl- |
| D、K+、Ba2+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol Cl2溶于水的过程中有2NA个电子转移 |
| B、在1L 0.1mol?L-1氟化钠溶液中含有F-数目为NA |
| C、1mol甲醇中含有C-H键的数目为3NA |
| D、10L pH=1的硫酸溶液中含有的H+数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeSO4溶液中加入H2O2溶液的反应:Fe2++2H2O2+4H+═Fe3++4H2O |
| B、泡沫灭火器的反应原理为:Al3++3HCO3-═Al(OH)3↓+3CO2↑ |
| C、向明矾水溶液中滴加氢氧化钡溶液使SO42-恰好完全沉淀的反应:2Ba2++Al3++2SO42-+3OH-═2BaSO4↓+Al(OH)3↓ |
| D、将溴单质与少量铁加热反应的生成物溶于水,通入足量氯气后发生的反应:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向硝酸钙溶液里滴加稀盐酸得到pH=4的溶液中:c(Ca2+)=c(N03-) |
| B、将0.2mol?L-1 NaA溶液和0.1mol?L-1盐酸等体积混合所得的碱性溶液中(A-为酸根离子):c(Na+)>c(A-)>c(Cl-)>c(OH-) |
| C、0.1mol/L NaAl02溶液中:c(Na+)>c(A102-)>c(OH-)>c(H+) |
| D、浓度均为0.1mo1?L-1的CH3COOH、CH3COONa的混合溶液中:2c(OH-)=2c(H+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
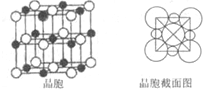 已知:A、B、C、D、E、F六种元素,原子序数依次增大.A原子核外有两种形状的电子云,两种形状的电子云轨道上电子相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素.试回答下列有关的问题:
已知:A、B、C、D、E、F六种元素,原子序数依次增大.A原子核外有两种形状的电子云,两种形状的电子云轨道上电子相等;B是短周期中原子半径最大的元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素.试回答下列有关的问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com