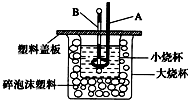
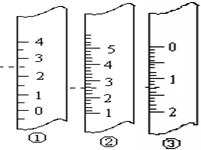
(1)如图所示为常见仪器的部分结构(有的仪器被放大)

D的仪器名称是______、A图中液面所示溶液的体积为______mL,C图中的液面与“0”刻度之间的体积差为______mL.(设A、C中分别盛有无色溶液).
(2)某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在容量瓶中配制A mL烧碱溶液
B.用移液管(或碱式滴定管)量取<“m“:math dsi:zoomscale=150 dsi:_mathzoomed=1>110
×A mL烧碱溶液于锥形瓶中并加几滴酚酞指示剂
C.在天平上准确称取烧碱样品wg,在烧杯中加蒸馏水溶解
D.将物质的量浓度为mmol/L的标准盐酸溶液装入酸式滴定管,调整液面,记下开始刻度V
1 mL
E.滴定到终点,记录终点刻度为V
2 mL
请完成下列问题:
①正确的操作步骤是(填写字母)______→______→______→D→______.
②操作中眼睛要注视______.
③滴定终点的判断______.
④若酸式滴定管没用标准盐酸润洗,会对测定结果有何影响______(填“偏高”、“偏低”或“无影响”,其他操作均正确).
⑤该烧碱样品的纯度计算式是______.