
下列叙述中不正确的是( )
A.颜色深浅:AgI>AgBr>AgCl
B.还原性:HF>HCl>HBr>HI
C.水溶液酸性:HI>HBr>HCl>HF
D.光敏性:AgI>AgBr>AgCl>AgF
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
下列关于元素周期表的叙述,错误的是( )
A.元素周期表揭示了化学元素间的内在联系,是化学发展史上的重要里程碑之一
B.在周期表中,把电子层数相同的元素排成一横行,称为一周期
C.元素周期表中,总共有18个纵行,18个族
D.第ⅠA族(除了H)的元素又称为碱金属元素,第ⅦA族的元素又称为卤族元素
查看答案和解析>>
科目:高中化学 来源: 题型:
如何除去下列物质中的杂质?(用化学方程式表示其过程)
(1)SiO2中混有CaCO3
________________________________________________________________________
(2)CaCO3中混有SiO2
________________________________________________________________________
(3)CO2中混有CO
________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种矿石,测定其含有的镁、硅、氧三种元素的质量比为12∶7∶16。
(1)用盐的组成表示其化学式:_____________________________________________;
(2)用氧化物的组成表示其化学式:_________________________________________;
(3)该矿石的成分属于________(填物质的分类)。
查看答案和解析>>
科目:高中化学 来源: 题型:
从海水中可以提取溴,主要反应为:2Br-+Cl2===Br2+2Cl-,下列说法正确的是( )
A.溴离子具有氧化性
B.氯气是还原剂
C.该反应属于复分解反应
D.氯气的氧化性比溴单质强
查看答案和解析>>
科目:高中化学 来源: 题型:
从海水中提取溴的方法之一是:
①向海水中通入Cl2;
②向所得的溶液中鼓入空气把溴吹出;
③用纯碱溶液吸收溴生成NaBr、NaBrO3;
④在上述溶液中加入稀硫酸使溴析出;
⑤加汽油、振荡、静置、分液。
根据以上叙述,回答下列问题:
(1)写出①中反应的离子方程式:__________________________________________
____________________。
(2)步骤②中利用了溴的性质有____________________________________________
____________________。
(3)④中反应的氧化剂是______________,还原剂是____________。
(4)能否将⑤中的汽油换成酒精?____________________________________
__________,原因是_____________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①能量越低的物质就越稳定;②白磷转化成红磷是放热反应。据此,下列判断或说法中正确的是(双选)( )
A.在相同的条件下,红磷比白磷稳定
B.在相同的条件下,白磷比红磷稳定
C.红磷和白磷的结构不同
D.红磷容易发生自燃而白磷则不会自燃
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到预期目的的是
| 编号 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸分别测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向10mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1 mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的Ksp: Mg(OH)2 >Fe(OH)3 |
| D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 证明非金属性S>C |
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W四种常见元素,且均为短周期元素。已知:①X的最高价氧化物对应的水化物为无机酸中最强酸;②Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料;③ Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料;④W被称为军事金属,可在CO2中燃烧。
(1)X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为
。
(2)Z的氧化物在通信领域用来作 ,工业上制Z单质的化学反应方程式为
。
(3)在50mL lmol·L-1的YX3溶液中逐滴加入0.5mol·L-1的NaOH溶液,得到1.56g沉淀,则加入NaOH溶液的体积最多为 mL。
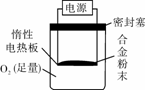
(4)Y、W合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某Y、W合金(设不含其他元素)中W的质量分数,设计下列实验方案进行探究。称量x g Y、W合金粉末,放在如右图所示装置的惰性电热板上,通电使其充分灼烧。欲计算W的质量分数。该实验中还需测定的数据是 。 若用空气代替O2进行实验,对测定结果是否有影响?若有影响分析其原因 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com