
将4gNaOH溶解在10mL水中,再稀释成1L,稀释后溶液的物质的量浓度是
A.1mol·L-1 B.0.1mol·L-1 C.0.001mol·L-1 D.10mol·L-1
科目:高中化学 来源:2016届浙江省高三上学期期中考试化学试卷(解析版) 题型:推断题
随原子序数的递增,八种短周期元素(用字母X等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)z在元素周期表的位置是 。
(2)比较d、f简单离子的半径大小(用化学符号表示,下同) > ;
比较d、g元素的简单气态氢化物的稳定性大小 > 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式 。
(4)已知1mol固体e的单质在足量d2气体中燃烧,恢复至室温,放出255.5kJ热量,写出该反应的热化学方程式 。
(5)由上述元素组成的离子化合物 Q:eh 和 W:e2gd4,若电解含2 molQ和2 molW的混合水溶液,当阳极产生44.8L气体(标准状况下,且不考虑气体的溶解和损失)时,电路中转移电子的物质的量为 mol。
(6)上述元素可组成盐R:zx4f(gd4)2。向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1 NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
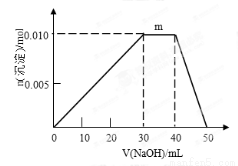
①R溶液中,离子浓度由大到小的顺序是 。
②写出m点发生反应的离子方程式 。
③若在R溶液中改加20mL 1.2 mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上第四次段考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法正确的是
A.1 mol Na2O2与SO2完全反应时转移电子数为NA
B.18g重水(D2O)所含的电子数为10NA
C.0. 5 mol NH4HSO4晶体中,含有H+数目约为0.5 NA
D.常温常压下,3gHCHO和CH3COOH的混合物中含有0.4NA个原子
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
A.元素W、X的氯化物中,各原子均满足8电子的稳定结构
B.元素X与氢形成的原子比为1:1的化合物有很多种
C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Z可与元素X形成共价化合物XZ2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西师范大学附属中学高三第一次模拟理化学试卷(解析版) 题型:实验题
海水中蕴藏着丰富的资源。海水综合利用的流程图如下。
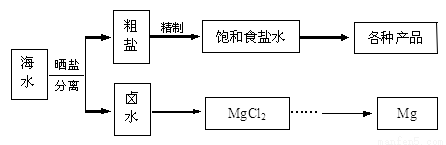
(1)粗盐中含Ca2+、Mg2+、Fe3+、SO42—及泥沙等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤; ⑦蒸发。正确的操作顺序是 (填写序号字母)。
A.⑤①③②④⑥⑦ B.⑤①②③⑥④⑦
C.⑤③①②⑥④⑦ D.⑤③②①⑥④⑦
(2)NaCl做原料可以得到多种产品。
①工业上由金属钠制备过氧化钠的方法是:将金属钠迅速升温至熔化,并控制温度在300–400℃,通入经处理过的空气可制得过氧化钠,处理空气的目的是 。工业生产中因温度过低而得不到纯净的过氧化钠,你认为可能含有的杂质是 (填化学式)。
② 实验室用惰性电极电解100 mL0.1 mol/LNaCl溶液,若阴阳两极均得到112 mL气体(标准状况),则所得溶液的pH为(常温下) (忽略反应前后溶液的体积变化)。
③ 电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式: 。
(3)分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品。
① 粗产品的溶液中含有Na+、Fe2+、Fe3+和Mn2+,需将Fe2+、Fe3+、Mn2+转化为沉淀除去。因此先向溶液中加入一种上述(1)中得到的物质NaClO,然后控制溶液的pH为 。
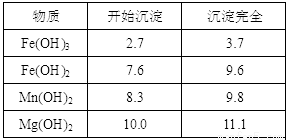
② 由MgCl2·6H2O晶体制备无水MgCl2的方法是 。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上学期12月第四次月考化学试卷(解析版) 题型:选择题
在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气。下列说法正确的是 ( )
A.甲烧杯中放入锌的质量比乙烧杯中放入锌的质量小
B.两烧杯中参加反应的锌等量
C.甲烧杯中的酸过量
D.反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高二上期中理化学卷(解析版) 题型:填空题
(1)在室温时,NaHSO4溶液中c(H+) c(OH-)+ c(SO42-)(填 “>”、“=”或“<”),硫酸氢钠溶液与氢氧化钡溶液反应,若溶液中SO42-完全沉淀,则反应后溶液的pH 7(填 “>”、“=”或“<”)。
(2)将20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为:  ;向此反应后的溶液中滴加0.01 mol·L-1BaCl2溶液,首先析出的沉淀是 。[KSP(BaSO4)=1.1×10-10mol2·L-2 ;KSP(BaCO3)=5.1×10-9mol2·L-2]
;向此反应后的溶液中滴加0.01 mol·L-1BaCl2溶液,首先析出的沉淀是 。[KSP(BaSO4)=1.1×10-10mol2·L-2 ;KSP(BaCO3)=5.1×10-9mol2·L-2]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com