
| A. | 乙烯在氧气中燃烧时放出热量,因此常用它来焊接或切割金属 | |
| B. | 乙二醇和丙三醇都是无色、黏稠、有甜味的液体,常用于配制化妆品 | |
| C. | 油脂在碱性条件下水解出的甘油常用于生产肥皂 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
分析 A.乙炔在氧气中燃烧放出大量的热,火焰温度高达3000℃以上,可用来焊接或切割金属,不是乙烯;
B.丙三醇常用于配制化妆品,乙二醇不是;
C.肥皂得主要成分为高级脂肪酸钠,甘油不能用于生产肥皂;
D.淀粉→葡萄糖→乙醇都是化学变化.
解答 解:A.工人师傅进行金属切割或焊接时使用的氧炔焰,是乙炔跟氧气发生氧化反应产生的火焰,故A错误;
B.乙二醇和丙三醇都是无色、黏稠、有甜味的液体,丙三醇具有吸湿性,能用作配制化妆瓶,乙二醇是制造涤纶的主要原料,也可作汽车发动机的抗冻剂,故B错误;
C.油脂为高级脂肪酸甘油酯,能够发生水解反应,则利用油脂在碱性条件下的水解反应生成的高级脂肪酸钠制取肥皂,不是水解产物甘油制取肥皂,故C错误;
D.用粮食酿酒时,先在糖化酶作用下水解为葡萄糖,然后在酒曲酒化酶的作用下转变为酒精,都是化学变化,故D正确;
故选D.
点评 本题主要考查了生活的化学相关的知识,掌握氧炔焰、乙二醇和丙三醇性质、肥皂成分、粮食酿酒等知识是解答的关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
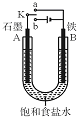 某课外活动小组同学用如图装置进行实验,试回答下列问题.
某课外活动小组同学用如图装置进行实验,试回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,五种元素原子半径从大到小的顺序是Na>Si>O>F>H (填元素符号);
,五种元素原子半径从大到小的顺序是Na>Si>O>F>H (填元素符号);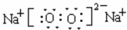 、
、 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃容器可长期盛放各种酸 | |
| B. | 纯碱可用于清洗油污 | |
| C. | 浓氨水可检验氯气管道泄漏 | |
| D. | 水玻璃是制备硅胶和木材防火剂的原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.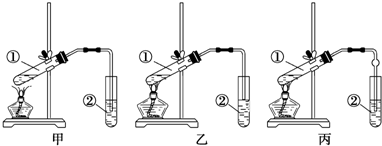
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液 | B. | KSCN溶液 | C. | NaOH溶液 | D. | NH3•H2O溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com