
已知常温下在溶液中可发生如下两个离子反应:
Ce4++Fe2+===Fe3++Ce3+
Sn2++2Fe3+===2Fe2++Sn4+
由此可确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是( )
A.Sn2+、Fe2+、Ce3+ B.Sn2+、Ce3+、Fe2+
C.Ce3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ce3+
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
已知X、Y、Z、W、K五种元素均位于周期表的前四周期,且原子序数依次增大。元素X是周期表中原子半径最小的元素;Y的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K位于ds区且原子的最外层电子数与X的相同。
请回答下列问题:(答题时,X、Y、Z、W、K用所对应的元素符号表示)
⑴Y、Z、W元素的第一电离能由大到小的顺序是 。
⑵K的电子排布式是 。
⑶Y、Z元素的某些氢化物的分子中均含有18个电子,则Y的这种氢化物的化学式是
;Y、Z的这些氢化物的沸点相差较大的主要原因是
 ⑷若X、Y、W形成的某化合物(相对分子质量为46)呈酸性,则该化合
⑷若X、Y、W形成的某化合物(相对分子质量为46)呈酸性,则该化合
物分子中Y原子轨道的杂化类型是 ;1 mol该分子中含有
σ键的数目是 。
⑸Z、K两元素形成的某化合物的晶胞结构如右图所示,则该化合物的
化学式是 ,Z原子的配位数是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
碘也可用作心脏起搏器电源——锂碘电池的材料。
该电池反应为2Li(s)+I2(s)===2LiI(s) ΔH
已知:4Li(s)+O2(g)===2Li2O(s) ΔH1
4LiI(s)+O2(g)===2I2(s)+2Li2O(s) ΔH2
则电池反应的ΔH=__________;碘电极作为该电池的________极。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中的药品常按物质的性质、类别等有规律地摆放。现有部分药品按某种规律摆放在实验桌上,如下图。做实验时,某同学取用硝酸溶液后,应把它放回的位置是( )

查看答案和解析>>
科目:高中化学 来源: 题型:
下列三组物质中,均有一种物质的类别与其他三种不同。
①MgO、Na2O、CO2、CuO ②HCl、H2O、H2SO4、HNO3 ③NaOH、Na2CO3、KOH、Cu(OH)2
(1)三种物质依次是(填化学式):A________;B________;C________。
(2)这三种物质相互作用可生成一种新物质NaHCO3,该反应________(“是”或“不是”)氧化还原反应。
(3)写出物质C与足量稀硫酸反应的离子方程式________________________________________。
(4)HCO 与H+、OH-在溶液中能共存吗?试用离子方程式说明____________________________________________________________________________________________________________________。
与H+、OH-在溶液中能共存吗?试用离子方程式说明____________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热
△H=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)===2CO(g)+O2(g)反应的
△H=+2×283.0kJ/mol
C.△H>0,△S>0,在任何温度下都不可自发进行。
D.1mol甲烷燃烧生成气态水和二氧化碳 所放出的热量是甲烷的燃烧热
所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨厂所需H2可由焦炭与水反应制得,其中有一步反应为CO(g)+H2O(g)==CO2(g)+H2(g) △H<0欲提高CO转化率,可采用的方法是( )
①降低温度; ②增大压强; ③使用催化剂;④增大CO浓度; ⑤增大水蒸气浓度
A.①②③  B.④⑤
B.④⑤  C.①⑤ D.⑤
C.①⑤ D.⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
由2 氯丙烷制取少量的1,2丙二醇(
氯丙烷制取少量的1,2丙二醇(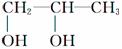 )时,需要经过下列哪几步反应
)时,需要经过下列哪几步反应
( )
A.加成→消去→取代 B.消去→加成→水解
C.取代→消去→加成 D.消去→加成→消去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com