
【题目】常见有机物A~D有下图转化关系(部分反应条件和部分产物已略去)。已知A是一种酯,其分子式为C4H8O2,B是食醋的主要成分。

请回答下列问题:
(1)写出C和D含有的官能团名称___________、_____________;
(2)写出B和D的结构简式___________、_____________;
(3)写出B和C生成A的化学方程式___________________________________。
【答案】羟基 醛基 CH3COOH CH3CHO CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
【解析】
A是一种酯,其分子式为C4H8O2,B是食醋的主要成分,则B为乙酸,C为乙醇,乙酸和乙醇发生酯化反应生成A,A为乙酸乙酯;C氧化生成D,D氧化生成B,乙醇D为乙醛,据此分析解答。
根据上述分析,A为乙酸乙酯,B为乙酸,C为乙醇,D为乙醛;
(1) C为乙醇,D为乙醛,含有的官能团分别为羟基和醛基,故答案为:羟基;醛基;
(2) B为乙酸,D为乙醛,结构简式分别为CH3COOH、CH3CHO,故答案为:CH3COOH;CH3CHO;
(3)乙酸和乙醇发生酯化反应生成乙酸乙酯,反应的化学方程式为CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,向1L 0.10mol/L的NaA溶被中,不断通入HCl气体(忽略溶液体积变化),得到c(A-)和c(HA)与pH的变化关系如下,则下列说法正确的是

A. 水的电离程度:X<Z
B. 溶液的pH比较:X<Y<Z
C. Y点时:c(Na+)=2c(A-)>c(H+)>c(OH-)
D. 常温下、HA的Ka=104.75
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分离提纯(括号内的物质为杂质)的方法错误的是( )
A.乙醇(水)--加入CaO蒸馏
B.NaCl(KNO3)--结晶和重结晶
C.乙酸乙酯(乙醇、乙酸)--饱和碳酸钠溶液,分液
D.己烷(己烯)--溴水,分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读体检报告呈现的的部分内容,判断下列说法不正确的是
项目名称 | 检查结果 | 单位 | 参考范围 |
钾 | 4.1 | mmol/L | 3.5~5.5 |
钙 | 2.15 | mmol/L | 2.13~2.70 |
胱抑素C | 0.78 | mg/L | 0.59~1.03 |
尿素 | 4.18 | mmol/L | 2.78~7.14 |
甘油三酯 | 1.50 | mmol/L | 0.45~1.70 |
A.体检指标均以物质的量浓度表示
B.表中所示的检查项目均正常
C.尿素是蛋白质的代谢产物
D.甘油三酯的结构可表示为![]() (R1、R2、R3为烃基)
(R1、R2、R3为烃基)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气吹出法工艺是目前“海水提溴”的最主要方法之一。其工艺流程如图所示,其中不正确的是
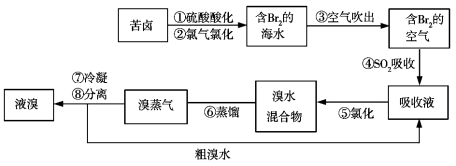
A.步骤④⑤是为了富集溴
B.步骤③说明溴具有挥发性
C.步骤④的离子方程式为Br2+SO2+H2O![]() 2H++2Br-+SO32-
2H++2Br-+SO32-
D.步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物可用分液漏斗分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
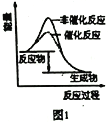
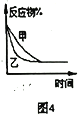
A. 图1表示分别在有、无催化剂的情况下某吸热反应过程中的能量变化
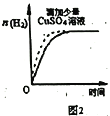
B. 图2表示常温下,等量锌粉与足量的等浓度的盐酸反应(滴加CuSO4溶液的为虚线)
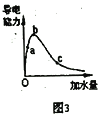
C. 图3表示mg冰醋酸加水稀释过程中溶液导电能力的变化,其中醋酸的电离度c>b>a
D. 图4表压强对合成氨反应的影响,乙的压强大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
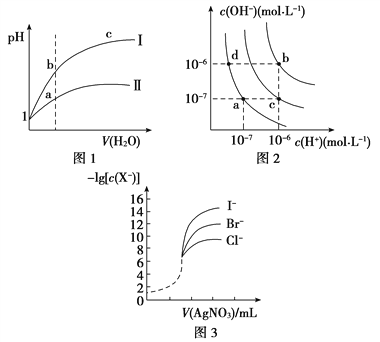
A. 图1表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强
B. 图2中纯水仅升高温度,就可以从a点变到c点
C. 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
D. 用0.010 0 mol/L硝酸银标准溶液,滴定浓度均为0.100 0 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)是一种无色易溶于水的油状液体,具有碱性和极强的还原性,在工业生产中应用非常广泛。
(1)肼(N2H4)是一种火箭燃料。已知:
N2(g)+2O2(g)=2NO2(g); △H=+67.7 kJ·mol-1
N2H4(g)+O(g)=N2(g)+2H2O(g); △H=-534.0 kJ·mol-1
NO2(g)=![]() N2O4(g); △H=-28.0 kJ·mol-1
N2O4(g); △H=-28.0 kJ·mol-1
反应2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g)的△H=________kJ·mol-1。
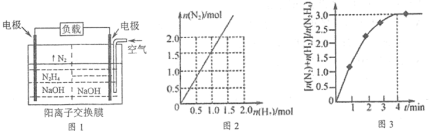
(2)目前正在研发的高能量密度燃料电池车是以水合肼燃料电池作为动力来源,电池结构如图1所示。
①起始时正极区与负极区NaOH溶液浓度相同,工作一段时间后,NaOH浓度较大的是___(填“正”或“负”)极区。
②该电池负极的电极反应式为_____________。
(3)已知水合肼是二元弱碱(25℃,K1=5×10-7,K2=5×10-15),0.1 mol·L-1水合肼溶液中四种离子:①H+、②OH-、③![]() 、④
、④![]() 的浓度从大到小的顺序为_________(填序号)。
的浓度从大到小的顺序为_________(填序号)。
(4)在弱酸性条件下水合肼可处理电镀废水,将![]() 还原为Cr(OH)3沉淀而除去,水合肼被氧化为N2,该反应的离子方程式为___________________。
还原为Cr(OH)3沉淀而除去,水合肼被氧化为N2,该反应的离子方程式为___________________。
(5)肼是一种优良的贮氢材料,其在不同条件下分解方式不同。
①在高温下,N2H4可完全分解为NH3、N2及H2,实验测得分解产物中N2与H2物质的量变化如图2所示,该分解反应方程式为__________________。
②在303K,NiPt催化下,则发生N2H4(l)![]() N2(g)+2H2(g)。在2L密闭容器中加入1 mol N2H4,测得容器中
N2(g)+2H2(g)。在2L密闭容器中加入1 mol N2H4,测得容器中![]() 与时间关系如图3所示。则0~4 min氮气的平均速率v(N2)=____________。
与时间关系如图3所示。则0~4 min氮气的平均速率v(N2)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2常用来漂白织物,其漂白能力是漂白粉的4~5倍NaClO2也是一种重要的杀菌消毒剂。工业上生产NaClO2的一种工艺流程如下图所示:

(1)ClO2发生器中的产品之一是NaHSO4,在该发生器中所发生反应的离子方程式为___________。
(2)反应结束后,向ClO2发生器中通入一定量空气,目的是___________。
(3)吸收器中发生反应的化学方程式为___________。吸收器中要用冷的NaOH溶液和H2O2溶液吸收CO2,原因是___________。
(4)将ClO2通入食盐水中,用情性电极电解,也可以制得NaClO2产品。阳极的电解产物是___________(填化学式),阴极的电极反应式为___________。
(5)相同条件下,1 mol NaClO2与___________gCl2的氧化能力相当。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com