
将固体NH4Br置于密闭容器中,在某温度下,发生下列可逆反应:
NH4Br(s)  NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g)  Br2(g)+H2(g)
Br2(g)+H2(g)
2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用v(NH3)表示,下列反应速率正确的是( )
A.0.5mol/(L·min) B.2.5 mol/(L·min)
C.2 mol/(L·min) D.5 mol/(L·min)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)
 nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
|
温度/℃ | 1 | 2 | 4 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是 ( )
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,44gCO2气体中含有的原子数为3NA
B.常温常压下,11.2 L 氯化氢气体中含有的分子数为0.5NA
C.1 mol铁与足量的稀硫酸完全反应转移的电子数为3NA
D.1 L 1 mol·L-1 CuCl2溶液中含有的氯离子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
.已知反应4CO(g)+2NO2(g) N2(g)+4CO2(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
N2(g)+4CO2(g)在不同条件下的化学反应速率如下,其中表示反应速率最快的是
A.v(CO)=1.5 mol·L-1·min-1 B.v(NO2)=0.7 mol·L-1·min-1
C.v(N2)=0.4 mol·L-1·min-1 D.v(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积不变的密闭容器中,一定条件下发生反应:2A(?) B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是( )
B(g)+2C(g),且达到平衡。当升高温度时气体的密度增大,则下列叙述中正确的是( )
A.升高温度,正反应速率增大,逆反应速率减小
B.若正反应是放热反应,则A为气态
C.物质A一定为非气态,且正反应是吸热反应
D.若向容器中充入惰性气体,则平衡向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下发生反应:
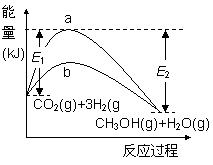
CO2(g)+3H2(g)  CH3OH(g)+H2O(g),右图表示该反应进行过程中的能量变化。
CH3OH(g)+H2O(g),右图表示该反应进行过程中的能量变化。
⑴图中曲线___(填“a”或“b”)表示使用催化剂时的反应进程。使用催化剂对该反应的影响是______(填选项字母)。
 A.提高反应速率
A.提高反应速率
B.提高CO2的转化率
C.降低反应活化能
D.改变反应的ΔH
 ⑵CO2(g)+3H2(g) CH3OH(g)+H2O(g)的化学平衡常数的表达式K=_______________________。升高温度,K值将_______(填“增大”、“减小”或“不变”)。
⑵CO2(g)+3H2(g) CH3OH(g)+H2O(g)的化学平衡常数的表达式K=_______________________。升高温度,K值将_______(填“增大”、“减小”或“不变”)。
⑶用含E1、E2的表达式表示
 CO2(g)+3H2(g) CH3OH(g)+H2O(g)的ΔH=______ kJ·mol-1
CO2(g)+3H2(g) CH3OH(g)+H2O(g)的ΔH=______ kJ·mol-1
⑷一定温度下,在体积为2L的容积固定的密闭容器中,充入2molCO2、6molH2,经10min反应达到平衡状态W,生成1molCH3OH。CO2的转化率为________。从反应开始到平衡,用H2的浓度变化表示的平均反应速率v(H2)=____________。该温度下,在体积为1L的容积固定的密闭容器中,从逆反应开始建立化学平衡,且各组分的平衡浓度与平衡状态W完全相同,则起始时充入容器的n(CH3OH)=________,n(H2O)=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语书写正确的是
A.纯碱溶液呈碱性的原因是:CO32-+2H2O H2CO3+2OH-
H2CO3+2OH-
B.电解MgCl2水溶液总的离子方程式:2Cl-+2H2O 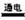 H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C.用电子式表示HCl的形成过程: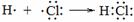
D.质量数之和是质子数之和两倍的水分子符号可能是:D218O
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸铁铵[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。
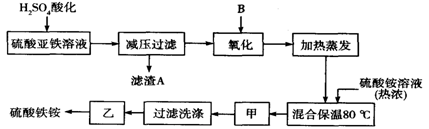
请回答下列问题:
(1)下列物质中最适合的氧化剂B是 ;
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
反应的离子方程式 。
(2)上述流程中,用足量最适合的氧化剂B氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,所加试剂为 (写名称),能否用酸性的KMnO4溶液? 理由是: 。(可用文字或方程式说明)
(3)检验硫酸铁铵中NH4+的方法是 。
(4)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入含0.05 mol Ba (NO3)2的溶液,恰好完全反应。则该硫酸铁铵的化学式为______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.SO2和NO2都是酸性氧化物,都能与水反应生成酸
B.Na20和Na202组成元素相同,与CO2反应产物也完全相同
C.Al203和Na20按物质的量比1:1投人水中可得到澄清溶液
D.金属铝排在金属活动性顺序表中氢元素的前面,铝与强酸反应一定放出氢气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com