
【题目】已知铍的原子序数为4,下列对铍及其化合物的叙述中,正确的是( )
A.铍的金属性比钠强
B.氯化铍的氧化性比氯化锂弱
C.氢氧化铍的碱性比氢氧化钙弱
D.单质铍易跟冷水反应生成H2
科目:高中化学 来源: 题型:
【题目】从化学键的角度分析,化学反应的过程就是反应物的化学键的断裂和生成物的化学键的形成过程。已知键能数据如下表:
化学键 | N≡N | N—H | H—H |
键能(kJ/mol) | 942 | 391 | b |
反应N2(g)+3H2(g) ![]() 2NH3(g);△H=-93kJ·mol-1。试根据表中所列键能数据计算b数值:( )
2NH3(g);△H=-93kJ·mol-1。试根据表中所列键能数据计算b数值:( )
A.551
B.437
C.558
D.160
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于某有机物的性质叙述不正确的是( )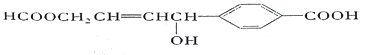
A.1 mol该有机物完全燃烧可生成12molCO2
B.1mol该有机物分别与足量Na或NaHCO3反应,产生的气体分子数目相等
C.1 mol该有机物可以与5mol H2发生加成反应
D.1 mol该有机物可以与2 molNaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的相对位置如图所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
X | Y | |
Z | W |
请回答下列问题:
(1)元素Z位于周期表中第_________周期_________族;
(2)这些元素的氢化物中,水溶液碱性最强的是_________(写化学式);
(3)XW2的电子式为_________;
(4)Y的最高价氧化物的化学式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】查阅医学资料,得知扁桃酸衍生物是重要的医药中间体,工业合成扁桃酸衍生物D路线如下:
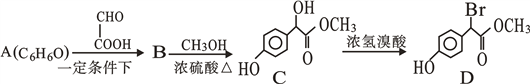
(1)A的结构式:_____。
(2)B含的官能团名称:_________ 。
(3) 写B生成C的化学方程式____________________________。
(4) C→D的反应类型是__________,1 mol D在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为_________mol。
(5)写出乙醛与A在一定条件下发生缩聚反应的化学方程式______________________(不要求指明反应条件)。
(6)同时符合下列条件的D的所有同分异构体(不考虑立体异构)有____种;
①能与NaHCO3溶液反应产生气体;
②苯环上只有2个取代基;
③遇氯化铁溶液发生显色反应。其中核磁共振氢谱显示为5组峰,且峰面积比为3:1:2:2:1的同分异构体是__________________(写结构简式)。
(7)已知: ,请设计合成路线以A和C2H2为原料合成
,请设计合成路线以A和C2H2为原料合成![]() (无机试剂任选):________________________。
(无机试剂任选):________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙醇、石墨和氢气的燃烧热分别为a、b、c(均为正值,单位均为kJ·mol-1)。则反应2C(s,石墨)+2H2(g)+H2O(l)==C2H5OH(l)的焓变为( )
A. (2b+2c-a) kJ·mol-1 B. (b+c-a) kJ·mol-1
C. (a-2b-2c) kJ·mol-1 D. (a-2b-c) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下(T2> Tl),在3个体积均为2.0 L的恒容密闭容器中反应 2NO(g)+ Cl2(g) = 2ClNO(g)(正反应放热)达到平衡,下列说法正确的是

A. 达到平衡时,容器I与容器II中的总压强之比为1:2
B. 达到平衡时,容器III中ClNO的转化率小于80%
C. 达到平衡时,容器II中c(ClNO(/ c(NO)比容器I中的大
D. 若温度为Tl,起始时向同体积恒容密闭容器中充入0.20 mol NO(g)、0.2 mol Cl2(g)和0.20 mol ClNO(g),则该反应向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可充电氟镁动力电池比锂电池具有更高的能量密度和安全性,在充电和放电时,其电池反应为Mg+2MnF3![]() 2MnF2+MgF2。下列说法不正确的是( )
2MnF2+MgF2。下列说法不正确的是( )
A. 放电时,镁为负极材料
B. 放电时,电子从镁极流出,经电解质流向正极
C. 充电时,阳极的电极反应式为:MnF2+F--e-=MnF3
D. 充电时,外加直流电源负极应与原电池的Mg极相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com