
| A、氧化还原反应:元素化合价是否变化 | B、纯净物与混合物:是否仅含有一种元素 | C、强弱电解质:溶液的导电能力大小 | D、溶液与胶体:本质不同的原因是能否发生丁达尔现象 |


 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:阅读理解
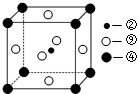
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化剂本身发生氧化反应 | B、既能与酸反应又能与碱反应的氧化物为两性氧化物 | C、实验室中常用排饱和食盐水的方法收集氯气,这一事实可以用平衡移动原理来解释 | D、“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com