
���� �ٽ������ˮ�õ���ɫ��Һ����CuCl2��
����������Һ�еμӹ���BaCl2��Һ���а�ɫ�������ɣ����ó����˳���������������ȫ����ϡHNO3����K2SO4��Ӧ����Na2CO3��
����ڵ���Һ�м���AgNO3��Һ���а�ɫ�������ɣ��ó���������ϡHNO3�����ɳ���ΪAgCl��������Ȼ���������֤������KCl��NaCl���Դ˽����⣮
��� �⣺�ٽ������ˮ�õ���ɫ��Һ����CuCl2��
����������Һ�еμӹ���BaCl2��Һ���а�ɫ�������ɣ����ó����˳���������������ȫ����ϡHNO3����K2SO4��Ӧ����Na2CO3��
����ڵ���Һ�м���AgNO3��Һ���а�ɫ�������ɣ��ó���������ϡHNO3�����ɳ���ΪAgCl��������Ȼ���������֤������KCl��NaCl��
��1�������Ϸ�����֪�϶�����Na2CO3���϶�û��CuCl2��K2SO4��ʵ��ڼ����Ȼ��������������ӣ�����֤���Ƿ���KCl��NaCl����Ŀû���漰KNO3������ʵ�飬��֤���Ƿ���KNO3���ʴ�Ϊ��Na2CO3��CuCl2��K2SO4��KCl��NaCl��KNO3��
��2�����з�Ӧ�����ӷ���ʽΪBa2++CO32-=BaCO3����BaCO3+2H+=Ba2++CO2��+H2O���ʴ�Ϊ��Ba2++CO32-=BaCO3����BaCO3+2H+=Ba2++CO2��+H2O��
���� ���⿼��������ƶϣ�Ϊ��Ƶ���㣬���հ�ɫ�����ijɷּ�ȷ��һ����̼����Ϊ���Ĺؼ��������������ʼ�������Ӧ�Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Դ�Ŀ����������������Ŀɳ�����չϢϢ��أ�
��Դ�Ŀ����������������Ŀɳ�����չϢϢ��أ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3��4 | B�� | 4��3 | C�� | 2��1 | D�� | 1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
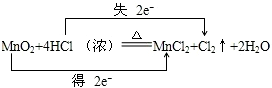 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BaSO4������ˮ��BaSO4���ڷǵ���� | |
| B�� | �ǵ���ʵ�ˮ��Һһ�������� | |
| C�� | �������Ҫ�������ᡢ��κͲ��������� | |
| D�� | ��������κ�����¾�һ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����� Cl2��Ӧ | B�� | ��ϩ�� Cl2��Ӧ | ||
| C�� | ��ϩ�� HCl ��Ӧ | D�� | ��ϩ�� H2��Cl2 ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʢ FeSO4��Һ����ƿ�ζ�ǰ�� FeSO4��Һ��ϴ 2-3 �� | |
| B�� | ѡ��ʽ�ζ���ʢ�ű� KMnO4��Һ�����õ⻯�ص�����Һ��ָʾ�� | |
| C�� | �ζ�ǰ���Ӷ������ζ����Ӷ����ᵼ�µζ����ƫ�� | |
| D�� | ��ƿ����Һ��ɫ�仯�ɻ�ɫ���ɫ���������µζ���Һ�����ڿ̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.5mol | B�� | 2mol | C�� | 2.5mol | D�� | 3mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ���������ˮ | B�� | ��CCl4 ��ȡ��ˮ�еĵ� | ||
| C�� | ����������NaOH��Һ | D�� | ����ˮ��Ͼ��ú�ֲ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com