
【题目】(1)根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
①该反应中氧化剂是 ,氧化产物是 。
②该反应中被氧化的物质与被还原的物质物质的量之比为 。
③用单线桥法标出点子转移的方向与数目。
(2)某一反应体系中存在下列6种物质:NO、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O.已知存在下列转化关系:HNO3→NO,请完成下列各题:
①该反应的氧化剂是 ,还原剂是 。
②该反应中1mol氧化剂 (填“得到”或“失去”) mol电子。
③当有0.1molHNO3被还原,此时生成标准状况下NO的体积是 L。
④请把各物质填在下面空格处,需配平:
□______+□______=□______+□______+□______+□
【答案】(1)①Cl2;N2②2:3③线桥略
(2)①HNO3;FeSO4②得到;3③2.24
④4HNO3+3FeSO4=Fe(NO3)3+Fe2(SO4)3+NO↑+2H2O
【解析】
试题分析:(1)①在氧化还原反应8NH3+3Cl2=6NH4Cl+N2中,氮元素化合价升高,被氧化,NH3作还原剂,N2是氧化产物;氯元素化合价降低,被还原,作氧化剂,NH4Cl是还原产物;故该反应的氧化剂是Cl2,还原剂是NH3;②若有8mol NH3参与反应,则2mol NH3被氧化,3mol Cl2被还原,因此该反应中被氧化的物质与被还原的物质物质的量之比为2:3;③氮元素失去6mole-,氯元素得到6mol e-,故单线桥从氮元素出发,到氯元素终止,据此利用单线桥法标出电子转移的方向和数目;(2)①由于反应中存在转化关系:HNO3→NO,因此氮元素化合价降低,被还原,HNO3为氧化剂,NO为还原产物;因此铁元素一定是化合价升高,被氧化,FeSO4是还原剂,Fe(NO3)3和Fe2(SO4)3是氧化产物;故该反应的氧化剂是HNO3,还原剂是FeSO4;②1mol氧化剂得到3mole-;③当有0.1molHNO3被还原,根据原子守恒可知,生成NO的物质的量为0.1mol,标准状况下的体积为![]() ;④根据得失电子守恒,并结合原子守恒,可以配平化学方程式:4HNO3+3FeSO4=Fe(NO3)3+Fe2(SO4)3+NO↑+2H2O 。
;④根据得失电子守恒,并结合原子守恒,可以配平化学方程式:4HNO3+3FeSO4=Fe(NO3)3+Fe2(SO4)3+NO↑+2H2O 。


科目:高中化学 来源: 题型:
【题目】我们日常生活中有“加碘食盐”、“增铁酱油”、“高钙牛奶”、“含氟牙膏”。这里的“碘”、“铁”、“钙”、“氟”指的是( )
A. 元素 B.单质 C.分子 D.氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性SO32->I-。某溶液中可能含有Na+、NH4+、Fe2+、K+、I-、SO32- 、SO42-,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判正确的是
A.肯定不含I- B.肯定含有Na+
C.肯定不含SO42-[来、:肯定含有SO32- D.不能肯定是否含有SO42
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图分别是温度计、量筒、滴定管的一部分,则:温度计应该是 ,读数是_______℃;量筒应该是 ,读数为 mL;滴定管应该是 ,读数为 mL 。



(2)用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列实验操作会引起测量结果偏高的是 。
①读取滴定管终点读数时,仰视刻度线。
②滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失
③中和滴定时,锥形瓶内有少量蒸馏水。
④酸式滴定管用蒸馏水洗后,未用标准液洗。
⑤用天平称量NaOH固体,将小烧杯放在右盘,砝码放在左盘,并移动游码,使之平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学一选修3:物质结构与性质】A、B、C、D、E五种元素的原子序数依次增大。A 是原子半径最小的元素;B的最外层电子数是次外层电子数的2倍; D的L能层有两对成对电子;E+的核外有三个能层,且都外于全满状态。试回答下列问题:
(1)基态E原子核外电子的排布式为___________________。
(2)B、C、D三种元素的电负性由大到小的顺序是____________(填元素符号)。A、C、D三种元素形成的常见离子化合物中阳离子的空间构型为_____________,阴离子的中心原子轨道采用______________杂化。
(3)E(CA3)![]() 离子的颜色是___________;含有化学键类型是_____________;离子中C原子杂化轨道类型是__________________。
离子的颜色是___________;含有化学键类型是_____________;离子中C原子杂化轨道类型是__________________。
(4)D、E能形成两种晶体,其晶胞分别如甲、乙两图。晶体乙中,E的配位数为_________;在一定条件下,甲和C2A4反应生成乙,同时生成在常温下分别为气体和液体的另外两种常见无污染物质。该化学反应方程式为______________________。

(5)若甲的密度为ρ g/cm3,NA表示阿伏加德罗常数,则甲晶胞的边长可表示为_________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以CuSO4溶液为电解质溶液进行粗铜(合Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
A. 电能全部转化为化学能
B. 反应溶液中Cu2+向阳极移动
C. 粗铜接电源正极,发生氧化反应
D. 利用阳极泥可回收Zn、Ag、Pt、Au等金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:C(s)+2H2(g)![]() CH4(g)。在VL的容器中投入amol碳(足量),同时通入2amol H2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示。下列说法不正确的是( )
CH4(g)。在VL的容器中投入amol碳(足量),同时通入2amol H2,控制条件使其发生上述反应,测得碳的平衡转化率随压强及温度的变化关系如下图所示。下列说法不正确的是( )
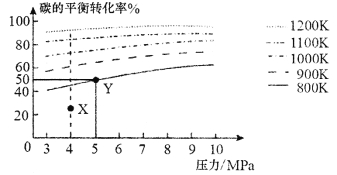
A.上述正反应为吸热反应
B.在4MPa、1200K时,图中X点v(H2)正>v(H2)逆
C.Y点H2的转化率为50%
D.工业上维持6MPa、1000K而不采用10MPa、1000K,主要是因为前者碳的转化率高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com