
根据下列实验现象,所得结论错误的是 
| 实验 | 实验现象 | 结论 |
| A | Ⅰ烧杯中铁片表面有气泡,Ⅱ烧杯中铜片表面有气泡 | 活动性:Al>Fe>Cu |
| B | 试管中收集到无色气体 | 铜与浓硝酸反应产物是NO |
| C | 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
| D | 长颈漏斗内液面高于烧瓶内液面且保持不变 | 装置气密性良好 |
B
解析试题分析:A、根据原电池的工作原理,左烧杯中铁表面有气泡,说明负极为铝,正极为铁,金属活动性Al>Fe,右边烧杯中铜表面有气泡,说明铁为负极,铜为正极,金属活动性Fe>Cu,则活动性为Al>Fe>Cu,故A正确;B、Cu与浓硝酸反应,反应中的化合价变化为:HNO3中N元素由+5价降低为NO2中N元素+4价,HNO3是氧化剂,NO2是还原产物,方程式为:Cu+4HNO3═Cu(NO3)2+2NO2↑+2H2O;生成的红棕色二氧化氮和水发生氧化还原反应,3NO2+H2O=2HNO3+NO,所以图中试管中收集到无色气体为一氧化氮,但不是铜和浓硝酸反应生成一氧化氮,故B错误;C、Fe3+遇SCN-发生反应Fe3++3SCN-?Fe(SCN)3,Fe(SCN)3为血红色,增大氯化铁溶液的浓度,根据溶液颜色变化来判断反应方向,如果溶液颜色加深,则说明平衡向正反应方向移动,所以能达到实验目的,故C正确;D、该装置的气密性检查,主要是通过气体压强增大看体积变化来进行检验,夹紧止水夹,向长颈漏斗中加水至其液面高于烧瓶内的液面,一段时间后,看液面高度差有无变化,变化说明装置漏气,反之不漏气,故D正确。
考点:常见气体制备原理及装置选择;原电池和电解池的工作原理;气体发生装置的气密性检查;探究浓度对化学平衡的影响 。


科目:高中化学 来源: 题型:单选题
用下列实验装置进行的实验中,不能达到相应实验目的的是 ( )
| A.装置甲:气体从b口进入,收集CO2 | B.装置乙:可制得金属锰 |
| C.装置丙:实验室制取乙酸乙酯 | D.装置丁:验证HCl气体在水中的溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述正确的是
| A.图I装置中通入N2和O2的作用是相同的 |
| B.图Ⅱ中甲、乙两装置产生喷泉的原理一样 |
| C.图Ⅲ①装置中镁片是原电池的负极;②装置中镁片是原电池的正极 |
| D.图Ⅳ分液漏斗盛硝酸能证明非金属性N>C>Si,盛硫酸能证明非金属性S>C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
以下进行性质比较的实验,不合理的是
| A.比较Cu、Fe2+的还原性:铁加入硫酸铜溶液中 |
| B.比较氯、溴单质的氧化性:溴化钠溶液中通入氯气 |
| C.比较镁、铝金属性:氯化镁、氯化铝溶液中分别加入过量的NaOH溶液 |
| D.比较碳、硫非金属性:测定同条件同物质的量浓度的Na2CO3、Na2SO4溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是
| | 操作 | 现象 | 结论 |
| A | 滴加BaC12溶液 | 生成白色沉淀 | 原溶液中有SO42― |
| B | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+无K+ |
| C | 滴加氯水和CC14,振荡、静置 | 下层溶液液显紫色 | 原溶液中有I― |
| D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
.[实验化学]
苯亚甲基苯乙酮俗称查尔酮,淡黄色棱状晶体,熔点58℃,沸点208℃(3.3kPa)易溶于醚、氯仿和苯,微溶于醇。制备原理如下: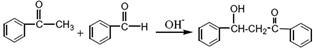
 (查尔酮)
(查尔酮)
(1)制备过程中,需在搅拌下滴加苯甲醛,并控制滴加速度使反应温度维持在25~30℃,说明该反应是 (填放热或吸热)反应。如温度过高时,则可以采取 措施。
(2)产品结晶前,可以加入几粒成品的查尔酮,其作用是 。
(3)结晶完全后,需抽滤收集产物。抽滤装置所包含的仪器除
减压系统外还有 、 (填仪器名称)。
(4)获得的深色粗产品加入活性炭,以95%乙醇重结晶。加入活性炭的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
从绿色化学的理念出发,下列实验不宜用下图所示装置进行的是( )。
| A.不同浓度的硝酸与铜反应 |
| B.稀硫酸与纯碱或小苏打反应 |
| C.铝与氢氧化钠溶液或盐酸反应 |
| D.H2O2在不同催化剂作用下分解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com