
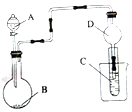
| A. | 若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,则C中产生白色沉淀,白色沉淀不会消失 | |
| B. | 实验仪器D可以起到防止溶液倒吸的作用 | |
| C. | 若A为浓盐酸,B为MnO2,C中盛石蕊溶液,则C中溶液先变红后褪色 | |
| D. | 若A为浓盐酸,B为贝壳,C中盛有硅酸钠溶液,则C中出现白色沉淀可证明酸性的强弱为:碳酸>硅酸 |
分析 A.若A为浓氨水,B为生石灰,二者混合得到氨气,氨气与氯化铝反应生成白色沉淀;
B.D中具有球形结构;
C.若A为浓盐酸,B为MnO2,加热反应生成氯气,氯气与水反应生成HCl、HClO,HClO具有漂白性;
D.若A为浓盐酸,B为贝壳,二者反应生成二氧化碳,但盐酸易挥发,盐酸与C中硅酸钠反应.
解答 解:A.若A为浓氨水,B为生石灰,二者混合得到氨气,氢氧化铝可溶于强碱,氨气与氯化铝反应生成白色沉淀,则C中产生白色沉淀,白色沉淀不会消失,故A正确;
B.D中具有球形结构,则仪器D可以起到防止溶液倒吸的作用,故B正确;
C.若A为浓盐酸,B为MnO2,加热反应生成氯气,氯气与水反应生成HCl、HClO,HClO具有漂白性,则C中溶液先变红后褪色,故C正确;
D.若A为浓盐酸,B为贝壳,二者反应生成二氧化碳,但盐酸易挥发,盐酸与C中硅酸钠反应,则不能比较碳酸、硅酸的酸性,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的性质、发生的反应和现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH (g)和 1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
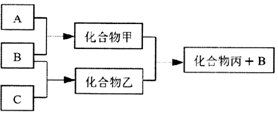 如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )| A. | Z元素位于第二周期第VIA族 | |
| B. | 可用排水法收集化合物乙 | |
| C. | 元素X、Y、Z的原子半径大小关系为X<Z<Y | |
| D. | 化合物甲溶于化合物丙中,存在的微粒有5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去Cl2的HCl气体可以通过浓硫酸 | |
| B. | 碳酸钠固体中的碳酸氢钠杂质可以通过加热除去 | |
| C. | SO2可以通过碱石灰干燥 | |
| D. | FeCl3溶液中含有CuCl2可以加入足量NaOH溶液除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl的摩尔质量是:74.5g | B. | 一水合氨的化学式为:NH4•OH | ||
| C. | Na2O2中的阴离子为:O2- | D. | 镁的原子结构示意图如图所示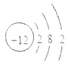 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
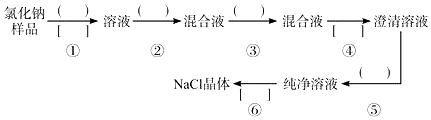
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以选用炭棒作为阴、阳极材料,但阳极材料也可以用铁棒 | |
| B. | 用湿润的淀粉KI试纸靠近阴极区域,试纸变蓝 | |
| C. | 电解过程中,在阴极区域溶液中滴加酚酞,溶液变红色 | |
| D. | 实验结束后将溶液搅拌,然后用pH试纸检验,溶液呈中性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com