
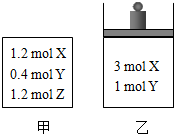
 在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3X(g)+Y(g)?2Z(g)△H<0,保持温度不变,测得平衡时的有关数据如下:下列说法正确的是( )
在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物(如图所示),发生如下反应:3X(g)+Y(g)?2Z(g)△H<0,保持温度不变,测得平衡时的有关数据如下:下列说法正确的是( )| 恒容容器甲 | 恒压容器乙 | |
| Y的物质的量/mol | n1 | n2 |
| Z的体积分数 | φ1 | φ2 |
| A. | 平衡时容器乙的容积一定比反应前大 | |
| B. | 平衡时容器甲的压强一定比反应前大 | |
| C. | n2>n1 | |
| D. | φ2>φ1 |
分析 将甲中Z完全转化为X和Y时,1.2molZ能转化为1.8molX、0.6molY,则X、Y的物质的量分别是3mol、1mol,所以与乙的初始状态是等效平衡,
该反应的正反应是一个反应前后气体体积减小的放热反应,甲恒容、乙恒压,乙在反应过程中与甲相比相当于增大压强,平衡正向移动,
A.乙中,温度和压强不变,容器中气体物质的量与体积成正比;
B.甲中,温度和条件不变,容器中气体压强与物质的量成正比;
C.甲恒容、乙恒压,乙在反应过程中与甲相比相当于增大压强,平衡正向移动,反应物转化率增大;
D.甲恒容、乙恒压,乙在反应过程中与甲相比相当于增大压强,平衡正向移动,生成物含量增大.
解答 解:将甲中Z完全转化为X和Y时,1.2molZ能转化为1.8molX、0.6molY,则X、Y的物质的量分别是3mol、1mol,所以与乙的初始状态是等效平衡,
该反应的正反应是一个反应前后气体体积减小的放热反应,甲恒容、乙恒压,乙在反应过程中与甲相比相当于增大压强,平衡正向移动,
A.乙中,温度和压强不变,容器中气体物质的量与体积成正比,平衡正向移动,气体的物质的量减小,则压强减小,所以平衡时容器乙的容积一定比反应前小,故A错误;
B.甲中,温度和条件不变,容器中气体压强与物质的量成正比,甲中反应向哪个方向移动还是平衡状态未知,所以无法确定气体物质的量任何变化,导致无法确定压强是否变化及如何变化,故B错误;
C.甲恒容、乙恒压,乙在反应过程中与甲相比相当于增大压强,平衡正向移动,反应物转化率增大,则Y的物质的量n2<n1,故C错误;
D.甲恒容、乙恒压,乙在反应过程中与甲相比相当于增大压强,平衡正向移动,生成物含量增大,所以φ2>φ1,故D正确;
故选D.
点评 本题考查化学平衡状态的有关判断,正确判断甲、乙存在等效平衡是解本题关键,知道P、V、T、n之间的关系,易错选项是B,题目难度中等.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:解答题
 CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料.
CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 酸性锌锰干电池是以锌筒作为负极,并经汞齐化处理,使表面性质更为均匀,以减少锌的腐蚀.正极材料是由二氧化锰粉、氯化铵及碳黑组成的一个混合糊状物.正极材料中间插入一根碳棒,作为引出电流的导体.由于酸性锰锌干电池制作简单、价格便宜,在干电池市场占有很大份额,但是他也具有一些致命的缺点;存放时间缩短,放电后电压下降较快等,因此废酸性锌猛干电池的综合利用非常重要.上图是某小型化工厂处理废干电池的流程简单示意图:
酸性锌锰干电池是以锌筒作为负极,并经汞齐化处理,使表面性质更为均匀,以减少锌的腐蚀.正极材料是由二氧化锰粉、氯化铵及碳黑组成的一个混合糊状物.正极材料中间插入一根碳棒,作为引出电流的导体.由于酸性锰锌干电池制作简单、价格便宜,在干电池市场占有很大份额,但是他也具有一些致命的缺点;存放时间缩短,放电后电压下降较快等,因此废酸性锌猛干电池的综合利用非常重要.上图是某小型化工厂处理废干电池的流程简单示意图:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
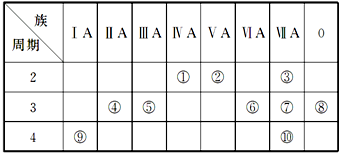
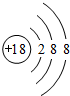 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v1>10v2 | |
| B. | 加少量水稀释,氨水中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$都减小 | |
| C. | v2≈v3 | |
| D. | 中和热A=B=C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油和天然气都属于碳素燃料 | |
| B. | 发展太阳能经济有助于减缓温室效应 | |
| C. | 太阳能电池可将太阳能转化为电能 | |
| D. | 目前研究菠菜蛋白质“发电”不属于“太阳能文明” |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+.
;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式):OH-、H3O+. Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18O是氧元素的一种核素,它的中子数是8 | |
| B. | O4和O2是互为同位素 | |
| C. | 同温同压下,等体积的O4气体和O2含有相同的分子数 | |
| D. | O4转化O2为物理性质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com