
设NA为阿伏加德罗常数的值。下列说法中,正确的是
A.1mol Na被氧化完全转化生成Na2O2,失去电子数为2NA
B.常温常压下,46g由NO2和N2O4组成的混合气体中含有原子的总数为3NA
C.将lmL 1 mol·L-1 FeCl3溶液逐滴加入沸水,制得红褐色Fe(OH)3胶体,所含胶粒的数目是1×10-3NA
D.标准状况下,6.72L NO2与足量水充分反应转移的电子数目为0.3NA
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2(g)⇌2AB2(g)(正反应放热),下列说法正确的( )
|
| A. | 升高温度,正向反应速率减小,逆向反应速率增加 |
|
| B. | 升高温度有利于反应速率增加,从而缩短达到平衡的时间 |
|
| C. | 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 |
|
| D. | 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组热化学方程式程中,化学反应的△H前者大于后者的是( )
①CaCO3(s)=CaO(s)+CO2(g)△H1 CaO(s)+H2O(l)=Ca(OH)2(s)△H2
②C(s)+O2(g)=CO2(g)△H3C(s)+1/2O2(g)=CO(g)△H4
③S(s)+O2(g)=SO2(g)△H5S(g)+O2(g)=SO2(g)△H6.
|
| A. | ①③ | B. | ①② | C. | ②③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NaHSO4在水中的电离方程式为NaHSO4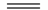 Na+ + H++
Na+ + H++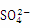 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。对于该溶液,下列叙述中不正确的是
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。对于该溶液,下列叙述中不正确的是
A.该温度高于25℃
B.水电离出来的c(H+)= 1×10-10 mol • L﹣1
C.c(H+)=c(OH-))+c(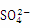 )
)
D.该温度下加入等体积pH为12的NaOH溶液可使反应后的溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
高氯酸三碳酰肼合镍{[Ni(CHZ)3](ClO4)2 }是一种新型的起爆药。
(1)Ni2+基态核外电子排布式为 。
(2)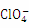 的空间构型是 ;与
的空间构型是 ;与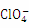 互为等电子体的一种分子为 (填化学式)。
互为等电子体的一种分子为 (填化学式)。
(3)化学式中CHZ为碳酰肼,组成为CO(N2H3)2,碳酰肼中碳原子的杂化轨道类型为 ;1molCO(N2H3)2分子中含有σ键数目为 。
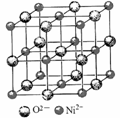
(4)高氯酸三碳酰肼合镍可由NiO、高氯酸及碳酰肼化合而成。NiO的晶胞结构如图所示,晶胞中含有的Ni2+数目为a,Ni2+的配位数为b,NiO晶体中每个镍离子距离最近的镍离子数目为c,则a∶b∶c= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某条件下,在2 L密闭容器中发生如下反应:2NO2(g)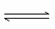 2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800 ℃,实验Ⅲ在850 ℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:
2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800 ℃,实验Ⅲ在850 ℃,NO、O2的起始浓度都为0,NO2的浓度(mol·L-1)随时间(min)的变化如图所示。请回答下列问题:

(1)实验Ⅱ隐含的反应条件是 。
(2)实验II中,从反应开始至达到平衡,用氧气浓度变化表示的化学反应速率为 。
(3)800 ℃时,该反应的平衡常数K= 。该反应是 (填“吸” 或“ 放”)热反应。
(4)若实验Ⅰ中达到平衡后,再向密闭容器中通入2 mol由物质的量之比为1∶1组成的NO2与O2混合气体(保持温度不变),此时反应将向 (填“正反应”或“逆反应”)方向进行。
(5)NO2、NO是重要的大气污染物,近年来人们利用NH3在一定条件下与之反应而将其转化为无害的参与大气循环的物质,如:8NH3+6NO2 7N2+12H2O。若将此反应设计成原电池,融熔K2CO3为电解质,则正极反应方程式为: 。
7N2+12H2O。若将此反应设计成原电池,融熔K2CO3为电解质,则正极反应方程式为: 。
(6)向AlCl3溶液中逐滴加入氨水,发生如下反应Al3++3NH3·H2O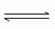 Al(OH)3↓+3
Al(OH)3↓+3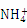 ,一般认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时,沉淀已完全。已知当溶液中Al3+恰好沉淀完全时溶液的pH=4.7,则Al(OH)3的溶度积常数为 (已知:lg2=0.3)。
,一般认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时,沉淀已完全。已知当溶液中Al3+恰好沉淀完全时溶液的pH=4.7,则Al(OH)3的溶度积常数为 (已知:lg2=0.3)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为元素周期表前四周期的一部分,下列有关R、W、X、 Y、Z五种元素的叙述中,正确的是
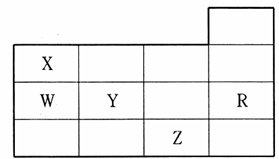
A.常压下,五种元素的单质中,Z单质的沸点最高
B.Y、Z的阴离子电子层结构都与R原子的相同
C.W的氢化物的沸点比X的氢化物的沸点高
D.Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同时,下列既能跟NaOH溶液反应,又能跟盐酸反应的溶液中,pH最大的是( )
|
| A. | Na2CO3溶液 | B. | NH4HCO3溶液 | C. | NaHCO3溶液 | D. | NaHSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 按系统命名法, |
|
| B. | 实验证实化合物 |
|
| C. | 能用新制的氢氧化铜鉴别乙醛与葡萄糖溶液 |
|
| D. | 化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com