
【题目】Ⅰ.已知C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ·mol-1 2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1,H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为_______。
Ⅱ.一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mo1)随时间t(min)的变化如图1所示。已知达平衡后,降低温度,A的体积分数将减小。

(1)该反应的化学方程式为___________________ 。
(2)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是____________。
②a、b、c三点中,C的体积分数最大的是________。
③各阶段的平衡常数如下表所示,则K1、K2、K3之间的大小关系为___________。
t2~t3 | t4~t5 | t5~t6 |
K1 | K2 | K3 |
【答案】+130 kJ/mol A+2B![]() 2C 升高温度 a K1>K2=K3
2C 升高温度 a K1>K2=K3
【解析】
I.根据盖斯定律计算水分解反应的焓变,化学反应的焓变△H=H(产物)-H(反应物),再结合化学键能和物质能量的关系来回答;
II.(1)根据图知,A、B为反应物而C为生成物,3min内△n(A)=(1-0.7)mol=0.3mol、△n(B)=(1-0.4)mol=0.6mol、△n(C)=(0.6-0)mol=0.6mol,相同时间内各物质的物质的量变化量之比等于其计量数之比,则A、B、C的计量数之比=0.3mol:0.6mol:0.6mol=1:2:2;
(2)①达平衡后,降低温度,A的体积分数将减小,说明降低温度,化学平衡正向移动,该反应的正反应为放热反应,t3时刻改变条件时正、逆反应速率都增大且逆反应速率大于正反应速率,平衡逆向移动;
②t3时刻平衡逆向移动,t5时刻正逆反应速率都增大但仍然相等,平衡不移动;
③该反应的正反应为放热反应,升高温度平衡逆向移动,化学平衡常数减小;温度不变,化学平衡常数不变。
I. 已知①C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ·mol-1>0,
②2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1
①×2-②得:2 H2O(g)=O2(g)+2H2(g) △H=(2a+220)kJmol-1>0,4×462-496-2×436=2a+220,
解得a=+130kJ/mol;
II.(1)根据图知,A、B为反应物而C为生成物,3min内△n(A)=(1-0.7)mol=0.3mol、△n(B)=(1-0.4)mol=0.6mol、△n(C)=(0.6-0)mol=0.6mol,相同时间内各物质的物质的量变化量之比等于其计量数之比,则A、B、C的计量数之比=0.3mol:0.6mol:0.6mol=1:2:2,最终各种物质都存在,且物质的量浓度不再发生变化,说明反应为可逆反应,该反应方程式为A+2B![]() 2C;
2C;
(2)①达平衡后,降低温度,A的体积分数将减小,说明降低温度,化学平衡正向移动,根据平衡移动原理:降低温度,平衡向放热反应分析移动,则该反应的正反应为放热反应,t3时刻改变外界条件时,正、逆反应速率都增大,且逆反应速率大于正反应速率,化学平衡逆向移动,则改变的条件是升高温度;
②t3时刻平衡逆向移动,t5时刻改变外界条件后,正、逆反应速率都增大但仍然相等,说明化学平衡不移动。平衡正向移动C的体积分数增大,平衡逆向移动,C的体积分数减小,所以a、b、c三点中C体积分数最大的是a点;
③该反应的正反应为放热反应,升高温度,平衡逆向移动,化学平衡常数减小;温度不变,化学平衡常数不变。由于反应温度:T(t2~t3)<T(t4~t5)=T(t5~t6),所以化学平衡常数K1>K2 =K3。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】处于平衡状态的反应:2H2S(g)![]() 2H2(g)+S2(g) ΔH>0,不改变其他条件的情况下,下列叙述正确的是( )
2H2(g)+S2(g) ΔH>0,不改变其他条件的情况下,下列叙述正确的是( )
A.加入催化剂,反应途径将发生改变,ΔH也将随之改变
B.升高温度,正、逆反应速率都增大,H2S分解率也增大
C.增大压强,平衡向逆反应方向移动,将引起体系温度降低
D.若体系恒容,注入一些H2后达新平衡,H2的浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)是一种片层状结构白色晶体,受热易分解。层内的 H3BO3分子通过氢键相连(如图所示),则下列有关说法中正确的是

A.正硼酸晶体属于原子晶体B.H3BO3分子的稳定性与氢键有关
C.1 mol H3BO3晶体中含有3 mol氢键D.分子中硼原子最外层为8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多,是一种常用的食品添加剂。该化合物具有如下性质:
(i)在25℃时,电离平衡常数K=3.9×10-4,K2=5.5×10-6
(ii)A+RCOOH(或ROH)![]()
![]() 有香味的产物
有香味的产物
(iii)1molA![]() 慢慢产生1.5mol气体
慢慢产生1.5mol气体
(iv)核磁共振氢谱说明A分子中有5种不同化学环境的氢原子与A相关的反应框图如下:

(1)依照化合物A的性质,对A的结构可作出的判断是___。
a.确信有碳碳双键 b.有两个羧基 c.确信有羟基 d.有-COOR官能团
(2)写出A、F的结构简式:A:__、F:__。
(3)写出A→B、B→E的反应类型:A→B___、B→E__。
(4)写出以下反应的反应条件:E→F第①步反应__。
(5)在催化剂作用下,B与乙二醇可发生缩聚反应,生成的高分子化合物用于制造玻璃钢。写出该反应的化学方程式:__。
(6)写出与A具有相同官能团的A的同分异构体的结构简式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
① 方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是________,此法的最大缺点是__________。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸、铜和氧化铁反应的化学方程式是_________________;向混合溶液中通入热空气的反应的离子方程式是___________________;由滤液得到无水硫酸铜的实验操作是______________。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:

①吸收塔中发生反应的化学方程式是_______________________。
② 有数据表明,吸收塔中溶液的pH在5.5~6.0之间,生产效率较高。当控制一定流量的尾气时,调节溶液的pH的方法是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计出一种可将光能转化为电能和化学能的天然气脱硫装置,如图,利用该装置可实现:H2S+O2 ═H2O2 +S。已知甲池中发生转化: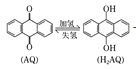 。下列说法错误的是
。下列说法错误的是
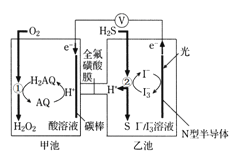
A.甲池碳棒上发生电极反应:AQ+2H++2e-=H2AQ
B.该装置工作时,溶液中的H+从甲池经过全氟磺酸膜进入乙池
C.甲池①处发生反应:O2+H2AQ=H2O2+AQ
D.乙池②处发生反应:H2S+I3-=3I-+S↓+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】373K时,某 1L密闭容器中加入2mol NH3发生如下可逆反应:2NH3(g)![]() N2(g)+3H2(g)。其中物质H2的物质的量变化如下图所示。
N2(g)+3H2(g)。其中物质H2的物质的量变化如下图所示。
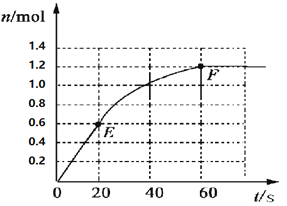
(1)前20 s内NH3(g)的平均反应速率为___________;
(2)373K时该反应的平衡常数的值为______________;
(3)若在此平衡体系中再加入1mol的NH3,与原平衡比较,新平衡时NH3的转化率______(填“增大”或“减小”,下同),NH3的平衡浓度_________。
(4)将原平衡升温至473K,重新达平衡时(其他条件不变),H2的平衡浓度为NH3的2倍,该反应的正反应为_________(填“放热反应”或“吸热反应”),为增大平衡体系中H2的物质的量,下列措施正确的是(其它条件相同)______。
a.升高温度 b.扩大容器的体积 c.加入合适的催化剂 d.再充入N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O![]() Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
A. 放电时负极附近溶液的碱性不变
B. 充电过程是化学能转化为电能的过程
C. 充电时阳极反应:Ni(OH)2-e-+ OH-=NiOOH + H2O
D. 放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀氨水中存在着下列平衡:NH3·H2O![]() NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
NH4++OH-,若要使平衡向逆反应方向移动,同时使c(OH-)增大,应加入的物质或采取的措施是
①NH4Cl固体;②硫酸;③NaOH固体;④水;⑤加热;⑥加入少量MgSO4固体。
A.①②③B.③⑥C.③D.③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com