
分析 利用反应速率与化学计量数的比值可知,比值越大,反应速率越快,以此来解答.
解答 解:利用反应速率与化学计量数的比值可知,比值越大,反应速率越快,
(1)$\frac{v(A)}{1}$=$\frac{0.3}{1}$mol/L•s=0.3mol/L•s,
(2)$\frac{v(B)}{3}$=$\frac{0.6}{3}$mol/L•s=0.2mol/L•s;
(3)$\frac{v(C)}{2}$=$\frac{0.4}{2}$mol/L•s=0.2mol/L•s;
(4)$\frac{v(D)}{2}$=$\frac{0.45}{2}$mol/L•s=0.225mol/L•s;
通过以上分析知,比值大小顺序是(1)>(4)>(2)=(3),所以反应速率快慢顺序是(1)>(4)>(2)=(3),
故答案为:(1)>(4)>(2)=(3).
点评 本题考查反应速率大小比较,为高频考点,明确化学反应速率与其计量数比值与反应速率快慢关系是解本题关键,注意比较反应速率大小时单位要统一,为易错点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:
五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息: ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA | |
| B. | 标准状况下,22.4 L一氯甲烷和二氯甲烷的混合物中所含的氯原子数介于NA至2NA之间 | |
| C. | 由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个 | |
| D. | 1mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
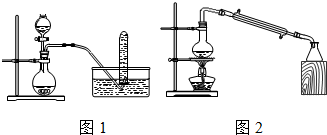
| A. | 铜与浓硝酸反应制取NO2可采用图1装置: | |
| B. | 图2实验装置设计正确,该装置可实现石油的分馏 | |
| C. | 分离乙酸和乙醇溶液:不能用分液漏斗进行分离 | |
| D. | 制乙酸乙酯时,把乙醇和乙酸依次加入浓硫酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ②
② ③
③ ④
④ ⑤
⑤
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28g乙烯(C2H4)中含有的π键数与13g乙炔(C2H2)中含有的π键数一样多 | |
| B. | 通过MnO2催化使H2O2分解,产生16g O2时转移电子数为2NA | |
| C. | 2.24L NH3中含共价键数目一定为0.3NA | |
| D. | 5.6g Fe投入100mL 3.5mol•L-1稀硝酸中,充分反应,转移电子总数为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10:7:11 | B. | 10:11:9 | C. | 10:11:8 | D. | 11:9:10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com